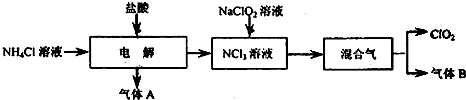
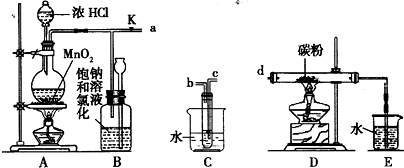
实验室常用强氧化剂(如KMnO4、KClO3和MnO2等)氧化浓盐酸的方法来制备氯气.某研究性学习小组欲探究用Na2O2与浓盐酸反应制备并检验氯气.供选用的实验试剂:a.Na2O2、b.浓盐酸、c.碱石灰、d.NaOH溶液、e.淀粉-KI溶液、f.CaCO3、g.石蕊试液、h.饱和NaCl溶液,装置如图所示(部分导管、蒸馏水略):
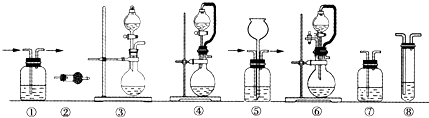
(1)写出用Na2O2与浓盐酸反应制备氯气的化学方程式: .
(2)下列装置组合最合理的是 (填序号,需考虑实验结束后拆卸装置时残留有害气体的处理).
(3)尾气经处理后仍有较多气体排出,其主要原因可用化学方程式表示为 .
(4)某小组成员建议用双氧水代替过氧化钠进行实验更好,请你给出两条合适的理由:① ,② .
(5)你是否同意将Na2O2与浓盐酸的反应作为实验室制备氯气的方法之一? (填“是”、“否”),理由是 .

(1)写出用Na2O2与浓盐酸反应制备氯气的化学方程式:
(2)下列装置组合最合理的是
| 组合 | 制备装置 | 净化装置 | 检验装置/试剂 | 尾气处理装置 |
| A | ③ | ② | ⑦/e | ⑤ |
| B | ③ | ① | ⑧/e | ① |
| C | ④ | ① | ⑤/e | ② |
| D | ⑥ | ⑤ | ⑧/e | ① |
(4)某小组成员建议用双氧水代替过氧化钠进行实验更好,请你给出两条合适的理由:①
(5)你是否同意将Na2O2与浓盐酸的反应作为实验室制备氯气的方法之一?
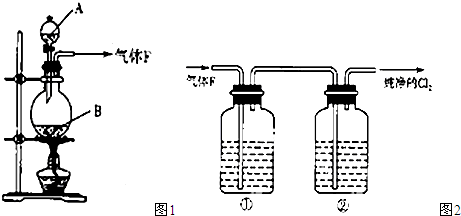
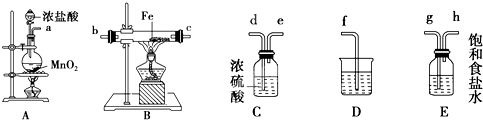
某小组同学用下图装置进行实验研究(a、b、c表示止水夹).请评价或完善其方案:
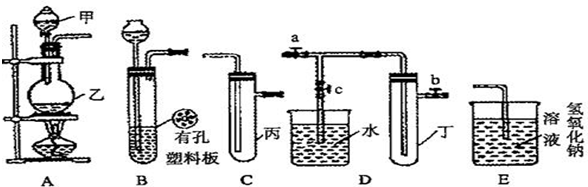
(1)用MnO2和浓盐酸制取氯气,将A、C、E相连,A中反应的离子方程式 .E中氢氧化钠溶液的作用 .
在丙中加入适量水可制得氯水.将所得氯水分成两份,进行实验,其操作、现象、结论为:
①实验I推出的相应结论是否合理? ,若不合理,请说明理由(若合理,无需填写): .
②实验II 推出的相应结论是否合理? ,若不合理,请说明理由(若合理,无需填写): .
(2)为比较Cl2和I2的氧化性强弱,将A、C、E相连,C中盛的试剂可以为 .
(3)将B、D、E装置相连后,在B中盛装浓硝酸和铜片(放在有孔塑料板上),可制得NO2并进行有关实验.
①B中发生反应的离子方程式为 .
②若关闭止水夹a、b,打开c,双手紧握(或微热)试管丁,使其中的NO2逸出进入D中,丁中可以观察到的现象 .
0 22068 22076 22082 22086 22092 22094 22098 22104 22106 22112 22118 22122 22124 22128 22134 22136 22142 22146 22148 22152 22154 22158 22160 22162 22163 22164 22166 22167 22168 22170 22172 22176 22178 22182 22184 22188 22194 22196 22202 22206 22208 22212 22218 22224 22226 22232 22236 22238 22244 22248 22254 22262 203614

(1)用MnO2和浓盐酸制取氯气,将A、C、E相连,A中反应的离子方程式
在丙中加入适量水可制得氯水.将所得氯水分成两份,进行实验,其操作、现象、结论为:
| 实验序号 | 实验操作 | 现象 | 结论 |
| Ⅰ | 将氯水滴入品红溶液 | 溶液褪色 | 氯气与水反应的产物有漂白性 |
| Ⅱ | 氯水中加入NaHCO3粉末 | 有无色气泡产生 | 氯气与水反应的产物具有较强的酸性 |
②实验II 推出的相应结论是否合理?
(2)为比较Cl2和I2的氧化性强弱,将A、C、E相连,C中盛的试剂可以为
(3)将B、D、E装置相连后,在B中盛装浓硝酸和铜片(放在有孔塑料板上),可制得NO2并进行有关实验.
①B中发生反应的离子方程式为
②若关闭止水夹a、b,打开c,双手紧握(或微热)试管丁,使其中的NO2逸出进入D中,丁中可以观察到的现象