化学一化学与技术
工业合成氨与制备硝酸一般可连续生产,流程如下:

请回答下列问题:
(1)工业生产时,制取氢气的一个反应为:
C0+H2O(g)?CO2+H2 t℃时,向 1L密闭容器中充入0.2molCO和0.3mol水蒸气.反应达到平衡后,体系中c(H2)=0.12mol?L-1,该温度下此反应的平衡常数K= (填计算结果).
(2)合成塔中发生反应N2(g)+3H2(g)?2NH3(g)△H<0.下表为不同温度下该反应的平衡常数.由此可推知,表中T1 573K (填“>”、“<”或“=”
(3)废水中的N、P元素是造成水体富营养化的关键因素,化工厂排放的废水中常含有较多的NH4+和PO43-,一般可以通过两种方法将其除去.
①方法一:将Ca(OH)2或CaO投加到待处理的废水中,生成磷酸钙从而进行回收.当处理后的废水中c(Ca2+)=2×10-7mol/L时,处理后的废水中c(PO43-)≤ mol/L.(已知Ksp[Ca3(PO4)2]=2×10-33)
②方法二:在废水中加入镁矿工业废水,就可以生成髙品位的磷矿石一鸟粪石,反应的离子方程式为Mg2++NH4++PO43-═MgNH4PO4↓.该方法中需要控制污水的pH为7.5?10,若pH高于10.7,鸟粪石的产量会大大降低.其原因可能为 ,与方法一相比,方法二的优点为 .
0 21973 21981 21987 21991 21997 21999 22003 22009 22011 22017 22023 22027 22029 22033 22039 22041 22047 22051 22053 22057 22059 22063 22065 22067 22068 22069 22071 22072 22073 22075 22077 22081 22083 22087 22089 22093 22099 22101 22107 22111 22113 22117 22123 22129 22131 22137 22141 22143 22149 22153 22159 22167 203614
工业合成氨与制备硝酸一般可连续生产,流程如下:

请回答下列问题:
(1)工业生产时,制取氢气的一个反应为:
C0+H2O(g)?CO2+H2 t℃时,向 1L密闭容器中充入0.2molCO和0.3mol水蒸气.反应达到平衡后,体系中c(H2)=0.12mol?L-1,该温度下此反应的平衡常数K=
(2)合成塔中发生反应N2(g)+3H2(g)?2NH3(g)△H<0.下表为不同温度下该反应的平衡常数.由此可推知,表中T1
| T/K | T1 | 573 | T2 |
| K | 1.00×107 | 2.45×105 | 1.88×103 |
①方法一:将Ca(OH)2或CaO投加到待处理的废水中,生成磷酸钙从而进行回收.当处理后的废水中c(Ca2+)=2×10-7mol/L时,处理后的废水中c(PO43-)≤
②方法二:在废水中加入镁矿工业废水,就可以生成髙品位的磷矿石一鸟粪石,反应的离子方程式为Mg2++NH4++PO43-═MgNH4PO4↓.该方法中需要控制污水的pH为7.5?10,若pH高于10.7,鸟粪石的产量会大大降低.其原因可能为

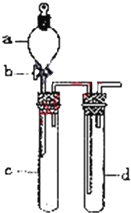 某兴趣小组设计出如右图所示装置来改进教材中“铜与硝酸反应”的实验,以探究化学实验的绿色化.
某兴趣小组设计出如右图所示装置来改进教材中“铜与硝酸反应”的实验,以探究化学实验的绿色化.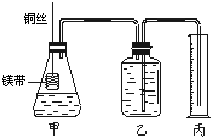 Ⅰ.铜与稀硝酸反应的离子方程式为
Ⅰ.铜与稀硝酸反应的离子方程式为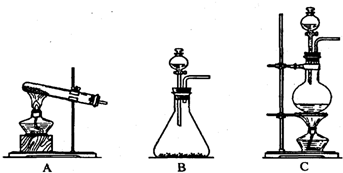
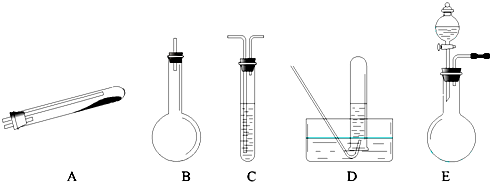
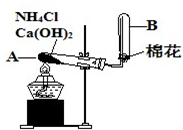 如图是实验室用氯化铵和熟石灰制取氨气的实验装置图.请回答以下各问题:
如图是实验室用氯化铵和熟石灰制取氨气的实验装置图.请回答以下各问题: