题目内容
汽车尾气中的NO是造成大气污染的物质之一,但NO又是工业生产硝酸的中间产物,另外NO在人体的血管系统内促进血管扩张作用,有三位教授因此项研究成果而获得诺贝尔奖.(1)下列选项与NOx对环境的污染无关的是
A.酸雨 B.赤潮 C.光化学烟雾 D.温室效应
(2)在汽车尾气排放管中安装一个催化转化器,可将尾气中另一种有害气体CO跟NO反应转化为无毒气体,该反应的化学方程式为
(3)氨气也可以用于处理氮氧化物,例如,氨气与二氧化氮发生如下反应:6NO2+8NH3=7N2+12H2O,标出反应的电子转移的数目和方向
(2)通过CO、NO结合产物为无毒气体信息分析,可以猜测出“无毒气体”的成分是N2和CO2;得到氧的物质是还原剂;失去氧的物质为氧化剂;
(3)在反应8NH3+6NO2=7N2+12H2O中,NH3→N2,化合价变化为-3价→0价,失8×3e-,NO2→N2,化合价变化为+4价→0价得6×4e-;
B.赤潮是由于水中的氮、磷元素浓度过大造成的水污染,与空气中的NOx对环境的污染无关,故B正确;
C.光化学污染来自于氮的氧化物和有机烃类在光作用下的一系列复杂变化;光化学烟雾,是城市大气中的碳氢化合物(HC)和氮氧化合物(NOx)在阳光紫外线的作用下发生的一系列链式大气化学反应生成以臭氧(O3)为代表的刺激性二次污染物,与NOx对环境的污染有关,故C错误;
D.温室效应是大量化石燃料燃烧导致产生大量二氧化碳的结果,与空气中的NOx对环境的污染无关,故D正确;
故答案为:BD;
(2)根据信息:使CO与NO反应,生成可参与大气生态循环的无毒气体N2和CO2,可知,CO和NO反应的化学方程式是:2NO+2CO
| ||
故答案为:2NO+2CO
| ||
(3)在反应8NH3+6NO2=7N2+12H2O中,NH3→N2,化合价变化为-3价→0价,NH3是还原剂,失8×3e-,NO2→N2,化合价变化为+4价→0价NO2是氧化剂,得6×4e-,可表示为
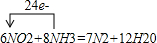 ,故答案为:
,故答案为: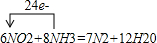 ;NH3;
;NH3;
 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案城市 | 污染指数 | 首要污染物 | 空气质量级别 |
北京 | 92 | TSP | Ⅱ |
天津 | 82 | TSP | Ⅱ |
太原 | 218 | TSP | Ⅳ |
长春 | 103 | TSP | Ⅲ |
哈尔滨 | 96 | TSP | Ⅱ |
上海 | 74 | NOx | Ⅱ |
南京 | 95 | TSP | Ⅱ |
杭州 | 67 | TSP | Ⅱ |
福州 | 42 |
| Ⅰ |
厦门 | 25 |
| Ⅰ |
济南 | 76 | TSP | Ⅱ |
武汉 | 83 | NO、NOx | Ⅱ |
广州 | 126 | NOx | Ⅲ |
深圳 | 77 | NOx | Ⅱ |
珠海 | 47 |
| Ⅰ |
汕头 | 54 |
| Ⅱ |
南宁 | 56 | TSP | Ⅱ |
成都 | 87 | TSP | Ⅱ |
重庆 | 98 | SOx | Ⅱ |
贵阳 | 69 | TSP | Ⅱ |
(TSP为空气中飘尘,NOx为含氮氧化物,SOx为硫的氧化物)
阅读分析上表,回答下列问题:
(1)经济特区中,空气质量最好的城市是_________,直辖市中空气质量最差的是__________。
(2)最容易出现酸雨的城市是_________,为防止城市出现酸雨,降低煤燃烧时向大气排放SO2,工业上将生石灰或石灰石和含硫煤混合使用。请写出燃烧时有关“固硫”(不使含硫化物进入大气)反应的化学方程式______________。
(3)你认为减少城市酸雨产生的途径可采取的措施是______________。
①少用煤作燃料 ②把工厂烟囱造高 ③燃料脱硫 ④在已酸化的土壤中加石灰 ⑤开发新能源
A.①②③ B.②③④⑤ C.①③⑤ D.①②③④
(4)北京市最近规定进京汽车尾气排放必须符合国家标准,因为汽车尾气(含烃类、CO、SO2与NO等有毒气体)是城市空气的污染源。治理的方法之一是在汽车的尾气排气管上装一个催化转换器(用Pt-Pd合金作催化剂),它的特点是使CO和NO反应,生成参与大气生态环境循环的无毒气体,并使汽油充分燃烧及SO2转化。
①写出NO和CO通过催化转换器发生反应的化学方程式________________。
②催化转换器的缺点是在一定程度上提高了空气的酸度。其原因是_____________。
③控制城市空气污染源的方法有( )
A.植树造林 B.开发氢能源
C.使用非机动车 D.控制汽车进城
E.使用无铅汽油