��Ŀ����
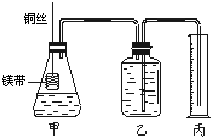 ��ͭ��ϡ���ᷴӦ�����ӷ���ʽΪ
��ͭ��ϡ���ᷴӦ�����ӷ���ʽΪ����ͭ��ϡ���ᷴӦ��ʵ��ʱ�����۲쵽�Թ������ɵ�������Ϊdz����ɫ����ԭ����
Ϊ����ֱ�ӹ۲쵽���ɵ��������ɫ��������ϡ�����м���ͭ��ͬʱ����������̼���Σ���ô��������̼���ε�������
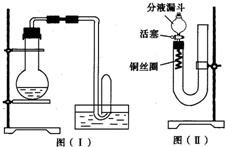
��ij�о���ѧϰС����֤������ͬ��ͬѹ�£���ͬŨ�ȡ���ͬ��������Բ�ͬ��һԪ��������þ����Ӧʱ�����������������ͬ����Ӧ���ʲ�ͬ��ͬʱ�ⶨʵ���������µ�����Ħ���������Ƶļ���ʵ��װ������ͼ��ʾ����ʵ�����Ҫ�����������£�
������Ũ�Ⱦ�Ϊ1mol?L-1����ʹ�����Һ��
����ȡ15.00mL 1mol?L-1����ʹ�����Һ�ֱ����������ƿ�У�
�۷ֱ��ȡ��ȥ��������Ĥ��þ��a g����ϵ��ͭ˿ĩ�ˣ�
���ڹ��ƿ��װ������ˮ����ͼ���Ӻ�װ�ã����װ�õ������ԣ�
�ݽ�ͭ˿�����ƶ���ʹ����þ���������У�ͭ˿������Ӵ���������Ӧ��ȫ����¼������ݣ�
��Ӧ��������¶Ȼָ������£������Һͱ���Һ��ʹ���ߴ���ͬһƽ�棬������Ͳ��ˮ�����ΪV mL��
�������ʵ�鲢�ش��������⣺
��1����ȡ15.00mL 1mol?L-1����ʹ�����Һ���õ�������
A�����̶ȵ��ձ� B����Ͳ C����ʽ�ζ��� D����ʽ�ζ���
��2���������a����ֵ������
��3����ʵ��װ�ñ�����Ͳ�Ĺ����
A��10mL B��100mL C��200mL D��500mL
��4����ˮ������Ӱ����Բ��ƣ���ʵ���������£�����Ħ������ļ���ʽΪ��Vm=
��5���Լ������ʲ��ȵ�ԭ����
��6����д��þ�������Һ��Ӧ�����ӷ���ʽ��
��������ͭ��ϡ���� ��Ӧ��������ͭ��һ��������ˮ���۲쵽�Թ������ɵ�������Ϊdz����ɫ����Ϊ�Թ��к��п�����һ����������������Ϊ����ɫ�����������������̼���λ�����ᷴӦ���ɶ�����̼������Թ��п����Ͼ������ڹ۲����ɵ���ɫһ���������壻
��1����ȡ15.00mL 1mol?L-1����ʹ�����Һ���õ������Ǿ�ȷ��Ϊ0.01ml����ʽ�ζ��ܣ�
��2�����ݻ�ѧ����ʽ��������þ������������װ��ѹǿ�仯��Һ��仯�����ж�װ�������ԣ��Ƚϻ�ѧ��Ӧ���ʣ������DZȽ�һ��ʱ��֮�ڵķ�Ӧ��Ũ�ȵı仯���������ı仯��
��3�����ݻ�ѧ����ʽ���м��㣻
��4����������Ħ�����Vm=
��������
��5����Ӱ�컯ѧ��Ӧ���ʵ�����������������þ��ͭ���γ�ԭ��أ��ӿ췴Ӧ���ʣ�����ʵ��ⶨ��
��6��þ�������Һ��Ӧ���ɴ���þ��������������������ʣ�
��1����ȡ15.00mL 1mol?L-1����ʹ�����Һ���õ������Ǿ�ȷ��Ϊ0.01ml����ʽ�ζ��ܣ�
��2�����ݻ�ѧ����ʽ��������þ������������װ��ѹǿ�仯��Һ��仯�����ж�װ�������ԣ��Ƚϻ�ѧ��Ӧ���ʣ������DZȽ�һ��ʱ��֮�ڵķ�Ӧ��Ũ�ȵı仯���������ı仯��
��3�����ݻ�ѧ����ʽ���м��㣻
��4����������Ħ�����Vm=
| V |
| n |
��5����Ӱ�컯ѧ��Ӧ���ʵ�����������������þ��ͭ���γ�ԭ��أ��ӿ췴Ӧ���ʣ�����ʵ��ⶨ��
��6��þ�������Һ��Ӧ���ɴ���þ��������������������ʣ�
����⣺��ͭ��ϡ���� ��Ӧ��������ͭ��һ��������ˮ����Ӧ�����ӷ���ʽΪ��3Cu+8H++2NO3-�T3Cu2++2NO��+4H2O���۲쵽�Թ������ɵ�������Ϊdz����ɫ����Ϊ�Թ��к��п�����һ����������������Ϊ����ɫ�����������������̼���λ�����ᷴӦ���ɶ�����̼������Թ��п����Ͼ������ڹ۲����ɵ���ɫһ���������壻
�ʴ�Ϊ��3Cu+8H++2NO3-�T3Cu2++2NO��+4H2O�� �Թ��ڴ��ڵĿ��������ɵ�NO����ΪNO2�� ̼����������ķ�Ӧ���ʿ죬���ɵ�CO2�������Թ��ڵĿ�����
��1������Ҫ��������10.00 mL�Ͼ�ȷ��Ӧѡ��ʽ�ζ��ܣ����ü�ʽ�ζ��ܻḯʴ�ܣ��ʴ�Ϊ��C��
��2��Mg+2HCl����HAc���TMgCl2+H2��
24g�� 2 mol����������������
a 1mol/L��0.015L����
a=0.18g��
����װ��ͼ������װ�������Լ��ķ����������ƽ�����ƿ��ڣ�����ȣ�һ�ᣬ��۲쵽���ƿ�г���������һ��ˮ������Һ�棬����װ�ò�©����
�Ƚϻ�ѧ��Ӧ���ʣ������DZȽ�һ��ʱ��֮�ڵķ�Ӧ��Ũ�ȵı仯���������ı仯��
�ʴ�Ϊ��0.18�������ƽ�����ƿ��ڣ�����ȣ�һ�ᣬ��۲쵽���ƿ�г���������һ��ˮ������Һ�棬����װ�ò�©������Ӧ��ֹʱ�䣻
��3��Mg+2HCl����HAc���TMgCl2+H2��
�� 2 mol����������������1 mol
�� 1 mol/L��0.015L���� n��H2��
n��H2��=0.0075 mol��V��H2��=0.0075 mol��22.4L/mol=0.168L=168ml��Ӧѡ200 mL��Ͳ��
�ʴ�Ϊ��C��
��4���ɣ�3������������ʵ���Ϊ0.0075 mol��ͨ������������ΪV mL��Vm=
=
=
L/mol���ʴ�Ϊ��
L/mol��
��5��Ӱ�컯ѧ��Ӧ���ʵ�������Ũ�ȡ��¶ȡ�ѹǿ�ȣ�����ΪŨ�Ȳ�ͬ��þ��ͭ���γ�ԭ��أ��ӿ췴Ӧ���ʣ�����ʵ��ⶨ������ͭ˿������Ӵ���
�ʴ�Ϊ�����Ũ����ͬʱ��c��H+����ͬ����ֹ���γ�ԭ��ض�����ʵ������Ĺ۲죻
��6��þ�������Һ��Ӧ���ɴ���þ��������������������ʣ�����þ������ˮ��ǿ����ʣ���Ӧ�����ӷ���ʽΪ��Mg+2CH3COOH=Mg2++2CH3COO-+H2����
�ʴ�Ϊ��Mg+2CH3COOH=Mg2++2CH3COO-+H2����
�ʴ�Ϊ��3Cu+8H++2NO3-�T3Cu2++2NO��+4H2O�� �Թ��ڴ��ڵĿ��������ɵ�NO����ΪNO2�� ̼����������ķ�Ӧ���ʿ죬���ɵ�CO2�������Թ��ڵĿ�����
��1������Ҫ��������10.00 mL�Ͼ�ȷ��Ӧѡ��ʽ�ζ��ܣ����ü�ʽ�ζ��ܻḯʴ�ܣ��ʴ�Ϊ��C��
��2��Mg+2HCl����HAc���TMgCl2+H2��
24g�� 2 mol����������������
a 1mol/L��0.015L����
a=0.18g��
����װ��ͼ������װ�������Լ��ķ����������ƽ�����ƿ��ڣ�����ȣ�һ�ᣬ��۲쵽���ƿ�г���������һ��ˮ������Һ�棬����װ�ò�©����
�Ƚϻ�ѧ��Ӧ���ʣ������DZȽ�һ��ʱ��֮�ڵķ�Ӧ��Ũ�ȵı仯���������ı仯��
�ʴ�Ϊ��0.18�������ƽ�����ƿ��ڣ�����ȣ�һ�ᣬ��۲쵽���ƿ�г���������һ��ˮ������Һ�棬����װ�ò�©������Ӧ��ֹʱ�䣻
��3��Mg+2HCl����HAc���TMgCl2+H2��
�� 2 mol����������������1 mol
�� 1 mol/L��0.015L���� n��H2��
n��H2��=0.0075 mol��V��H2��=0.0075 mol��22.4L/mol=0.168L=168ml��Ӧѡ200 mL��Ͳ��
�ʴ�Ϊ��C��
��4���ɣ�3������������ʵ���Ϊ0.0075 mol��ͨ������������ΪV mL��Vm=
| V |
| n |
| 0.001V |
| 0.0075 |
| V |
| 1000��0.0075 |
| V |
| 1000��0.0075 |
��5��Ӱ�컯ѧ��Ӧ���ʵ�������Ũ�ȡ��¶ȡ�ѹǿ�ȣ�����ΪŨ�Ȳ�ͬ��þ��ͭ���γ�ԭ��أ��ӿ췴Ӧ���ʣ�����ʵ��ⶨ������ͭ˿������Ӵ���
�ʴ�Ϊ�����Ũ����ͬʱ��c��H+����ͬ����ֹ���γ�ԭ��ض�����ʵ������Ĺ۲죻
��6��þ�������Һ��Ӧ���ɴ���þ��������������������ʣ�����þ������ˮ��ǿ����ʣ���Ӧ�����ӷ���ʽΪ��Mg+2CH3COOH=Mg2++2CH3COO-+H2����
�ʴ�Ϊ��Mg+2CH3COOH=Mg2++2CH3COO-+H2����
����������Ϊʵ��̽���⣬ע��ʵ�����������ע�����֪ʶ�����գ��Ѷ��еȣ�

��ϰ��ϵ�д�
�����Ŀ


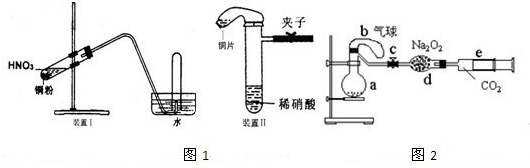
 ʵ������ϡ������Cu��Ӧ���Ʊ�NO���������ͼ����װ�ã�������ƿ�ڵĿ��������ų������ɵ�NO�ܿ챻�����ɺ���ɫ��NO2�����۲쵽����ɫ��NO���ɣ���ʹ������ˮ���ռ�����ɫ��NO��Ҳ��˵����������ΪNO����NO2��H2O��Ӧ���ɵģ����������ͼ����װ�ã���������ʵ����Դﵽ�����Ч����
ʵ������ϡ������Cu��Ӧ���Ʊ�NO���������ͼ����װ�ã�������ƿ�ڵĿ��������ų������ɵ�NO�ܿ챻�����ɺ���ɫ��NO2�����۲쵽����ɫ��NO���ɣ���ʹ������ˮ���ռ�����ɫ��NO��Ҳ��˵����������ΪNO����NO2��H2O��Ӧ���ɵģ����������ͼ����װ�ã���������ʵ����Դﵽ�����Ч����