碳酸钠、碳酸氢钠是两种重要的化学试剂.根据要求回答:
Ⅰ.兴趣小组设计三种方案,鉴别浓度均为0.01mol?L-1碳酸钠和碳酸氢钠两种溶液:
(1)甲方案中pH较大的是 ;
(2)结果表明方案乙无法实现鉴别目的,用离子方程式表示方案乙发生的反应: ; .
(3)经过查阅资料获得如下信息:Ksp(CaCO3)=4.96×10-9;0.01mol?L-1 NaHCO3、Na2CO3溶液中
c(CO32-)如表所示:
丙方案能否实现鉴别目的? ;理由是 ;
Ⅱ.纯碱生产过程中,所得产品往往混有一定量的氯化钠.为检测纯碱的纯度,可采用多种方案来进行.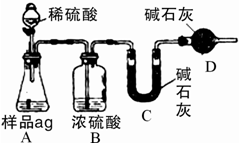
(4)如图为学生丁设计的方案,试图通过测定样品(a g)与足量的稀硫酸反应产生的CO2质量来实现目的.
①本方案存在缺陷,对纯碱纯度检测的影响.
缺陷: ;所测纯碱的纯度将 (填“偏大”或“偏小”).
②方案经改进后,丁进行了实验,并测得B、C、D三套装置的质量分别增重了m1、m2和m3.则纯碱的纯度为 .
(5)现只有少量(约1g)纯碱样品、0.100mol?L-1硫酸和蒸馏水,同学戊拟通过测定一定质量的纯碱样品与硫酸反应时消耗硫酸体积来确定纯碱的纯度.实验过程中,需用 (填仪器名称)测量硫酸的体积,而且实验过程中还需用到的一种试剂是 .
Ⅰ.兴趣小组设计三种方案,鉴别浓度均为0.01mol?L-1碳酸钠和碳酸氢钠两种溶液:
| 序号 | 甲 | 乙 | 丙 |
| 方案 | 用广泛pH试纸 检测溶液pH |
滴加等体积0.1mol?L-1 Ba(OH)2溶液 |
滴加等体积0.1mol?L-1 CaCl2溶液 |
(2)结果表明方案乙无法实现鉴别目的,用离子方程式表示方案乙发生的反应:
(3)经过查阅资料获得如下信息:Ksp(CaCO3)=4.96×10-9;0.01mol?L-1 NaHCO3、Na2CO3溶液中
c(CO32-)如表所示:
| 0.01mol?L-1溶液 | NaHCO3 | Na2CO3 |
| c(CO32-)/mol?L-1 | 0.00011 | 0.0087 |
Ⅱ.纯碱生产过程中,所得产品往往混有一定量的氯化钠.为检测纯碱的纯度,可采用多种方案来进行.

(4)如图为学生丁设计的方案,试图通过测定样品(a g)与足量的稀硫酸反应产生的CO2质量来实现目的.
①本方案存在缺陷,对纯碱纯度检测的影响.
缺陷:
②方案经改进后,丁进行了实验,并测得B、C、D三套装置的质量分别增重了m1、m2和m3.则纯碱的纯度为
(5)现只有少量(约1g)纯碱样品、0.100mol?L-1硫酸和蒸馏水,同学戊拟通过测定一定质量的纯碱样品与硫酸反应时消耗硫酸体积来确定纯碱的纯度.实验过程中,需用
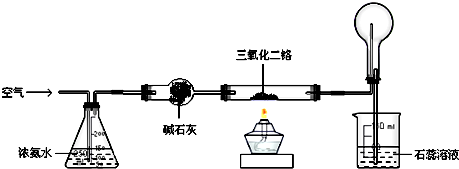
Ⅰ:某兴趣小组欲在绿色环保的条件下探究大气污染物SO2的性质,设计如图实验装置.请回答:
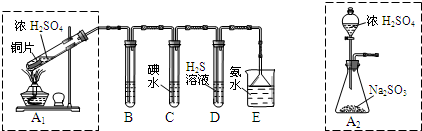
(1)B、C、D分别用于检验SO2的漂白性、还原性和氧化性,则B中所盛试剂为 ;C中反应的离子方程式为 .
(2)为了实现绿色环保的目标,某同学设计了上图A2的制取装置来代替A1装置,与A1装置相比,A2装置的优点是 (写2点).
Ⅱ:用氨水吸收尾气中的SO2,“吸收液”中可能含有OH-、SO
、SO
、HSO
等阴离子.请回答:
(3)氨水吸收过量SO2的反应的离子方程式为 .
(4))已知亚硫酸氢盐一般易溶于水,SO2也易溶于水.现有仪器和试剂为:小烧杯、试管、玻璃棒、胶头滴管、过滤装置和滤纸;2mol/L盐酸、2mol/L HNO3、1mol/L BaCl2溶液、1mol/L Ba(OH)2溶液、品红溶液、蒸馏水.请设计实验证明“吸收液”中存在SO
、HSO
,完成下表的实验操作、预期现象和结论:

(1)B、C、D分别用于检验SO2的漂白性、还原性和氧化性,则B中所盛试剂为
(2)为了实现绿色环保的目标,某同学设计了上图A2的制取装置来代替A1装置,与A1装置相比,A2装置的优点是
Ⅱ:用氨水吸收尾气中的SO2,“吸收液”中可能含有OH-、SO
2- 3 |
2- 4 |
- 3 |
(3)氨水吸收过量SO2的反应的离子方程式为
(4))已知亚硫酸氢盐一般易溶于水,SO2也易溶于水.现有仪器和试剂为:小烧杯、试管、玻璃棒、胶头滴管、过滤装置和滤纸;2mol/L盐酸、2mol/L HNO3、1mol/L BaCl2溶液、1mol/L Ba(OH)2溶液、品红溶液、蒸馏水.请设计实验证明“吸收液”中存在SO
2- 3 |
- 3 |
| 实验操作 | 预期现象与结论 | ||||
| 步骤1:取适量“吸收液”于小烧杯中,用胶头滴管取1mol/L BaCl2溶液向小烧杯滴加直至过量. | 若出现白色浑浊,则溶液中存在 SO
| ||||
| 步骤2:将小烧杯中的浊液过滤、洗涤,再用适量水把附在滤纸上的固体冲入另一小烧杯中;向冲下的固体 |
|||||
| 步骤3: |
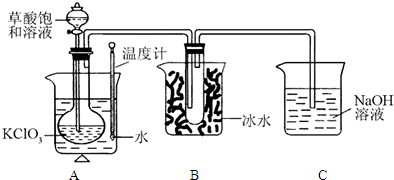
用如图装置进行SO2转化为SO3的转化率测定实验: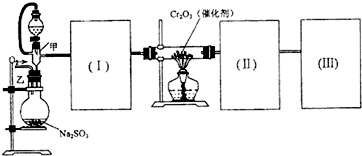
2SO2+O2
2SO3;△H=-196kJ/mol.已知:
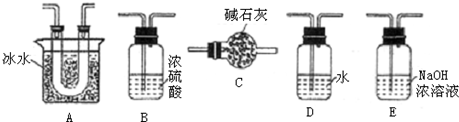
(1)要顺利进行实验,上图Ⅰ、Ⅱ、Ⅲ处各应连接合适的装置(可重复使用),请从下列A~E中选择适宜的装置,将其序号填入空格内.Ⅰ 、Ⅱ 、Ⅲ
(2)将装置连接好,实验前,必须进行的操作是(不必写具体过程) .
(3)实验时,浓硫酸能顺利滴入烧瓶中,甲装置所起的作用是 .解释实验室要用75%的浓硫酸而不用稀硫酸制备SO2的原因
(4)开始实验时,先从乙处均匀通入O2,为使SO2有较高的转化率,实验时滴入浓硫酸与加热催化剂的先后顺序是 .
(5)实验中“当Cr2O3表面红热时,应将酒精灯移开一会儿再加热”,以防温度过高,这样做的原因是 ;
(6)实验时若用25.2g的Na2SO3,加入的浓硫酸是足量的,反应结束时继续通入O2一段时间,称得Ⅱ处装置的质量增加11.3g,则本实验中SO2的转化率为 %(保留小数点后一位).
0 21970 21978 21984 21988 21994 21996 22000 22006 22008 22014 22020 22024 22026 22030 22036 22038 22044 22048 22050 22054 22056 22060 22062 22064 22065 22066 22068 22069 22070 22072 22074 22078 22080 22084 22086 22090 22096 22098 22104 22108 22110 22114 22120 22126 22128 22134 22138 22140 22146 22150 22156 22164 203614


2SO2+O2
| Cl2O2 |
| 熔点(℃) | 沸点(℃) | |
| SO2 | -72.4 | -10 |
| SO3 | 16.8 | 44.3 |
(2)将装置连接好,实验前,必须进行的操作是(不必写具体过程)
(3)实验时,浓硫酸能顺利滴入烧瓶中,甲装置所起的作用是
(4)开始实验时,先从乙处均匀通入O2,为使SO2有较高的转化率,实验时滴入浓硫酸与加热催化剂的先后顺序是
(5)实验中“当Cr2O3表面红热时,应将酒精灯移开一会儿再加热”,以防温度过高,这样做的原因是
(6)实验时若用25.2g的Na2SO3,加入的浓硫酸是足量的,反应结束时继续通入O2一段时间,称得Ⅱ处装置的质量增加11.3g,则本实验中SO2的转化率为
 氮的氧化物和SO2是常见的化工原料,但也是大气的主要污染物.综合治理其污染是化学家研究的主要内容.根据题意完成下列各题:
氮的氧化物和SO2是常见的化工原料,但也是大气的主要污染物.综合治理其污染是化学家研究的主要内容.根据题意完成下列各题: