题目内容
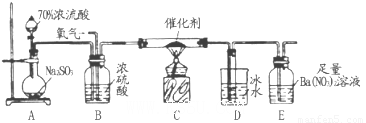
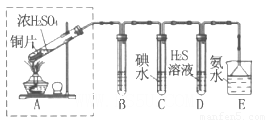
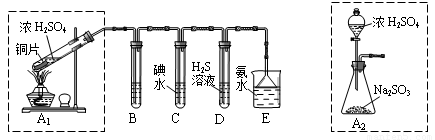
Ⅰ:某兴趣小组欲在绿色环保的条件下探究大气污染物SO2的性质,设计如图实验装置.请回答: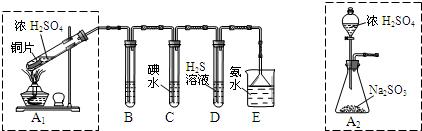
(1)B、C、D分别用于检验SO2的漂白性、还原性和氧化性,则B中所盛试剂为
(2)为了实现绿色环保的目标,某同学设计了上图A2的制取装置来代替A1装置,与A1装置相比,A2装置的优点是
Ⅱ:用氨水吸收尾气中的SO2,“吸收液”中可能含有OH-、SO
2- 3 |
2- 4 |
- 3 |
(3)氨水吸收过量SO2的反应的离子方程式为
(4))已知亚硫酸氢盐一般易溶于水,SO2也易溶于水.现有仪器和试剂为:小烧杯、试管、玻璃棒、胶头滴管、过滤装置和滤纸;2mol/L盐酸、2mol/L HNO3、1mol/L BaCl2溶液、1mol/L Ba(OH)2溶液、品红溶液、蒸馏水.请设计实验证明“吸收液”中存在SO
2- 3 |
- 3 |
| 实验操作 | 预期现象与结论 | ||||
| 步骤1:取适量“吸收液”于小烧杯中,用胶头滴管取1mol/L BaCl2溶液向小烧杯滴加直至过量. | 若出现白色浑浊,则溶液中存在 SO
| ||||
| 步骤2:将小烧杯中的浊液过滤、洗涤,再用适量水把附在滤纸上的固体冲入另一小烧杯中;向冲下的固体 |
|||||
| 步骤3: |
(2)依据装置图对比分析不同,总结优点;
(3)过量二氧化硫和氨水反应生成亚硫酸氢铵;
(4)依据SO32-和HSO3-离子的性质和检验方法设计实验进行检验设计;结合题干信息和条件,取少量于小烧杯中加入过量氯化钡反应生成沉淀为亚硫酸钡或硫酸钡沉淀;取沉淀加入酸的生成二氧化硫,通过检验二氧化硫的存在方法验证亚硫酸根离子的存在;取滤液依据亚硫酸氢根离子和酸反应可以生成二氧化硫,检验二氧化硫完成实验设计,或通过亚硫酸氢根离子和氢氧化钡反应生成沉淀分析判断;
故答案为:品红溶液; SO2+I2+2H2O═SO42-+2I-+4H+;
(2)装置图分析可知,A2的制取装置来代替A1装置,可以不需要加热或节约能源或药品,用分液漏斗加入硫酸可以控制反应速率,易于控制反应进行;或反应更充分,
故答案为:不用加热或节约能源或药品;或相对安全;或易于控制反应进行;或反应更充分;
(3)氨水吸收过量SO2的反应的离子方程式为NH3?H2O+SO2═NH4++HSO3-;
故答案为:NH3?H2O+SO2═NH4++HSO3-;
(4)依据SO32-和HSO3-离子的性质和检验方法设计实验进行检验设计;结合题干信息和条件,取少量于小烧杯中加入过量氯化钡反应生成沉淀为亚硫酸钡或硫酸钡沉淀;取沉淀加入酸的生成二氧化硫,通过检验二氧化硫的存在方法验证亚硫酸根离子的存在;取滤液依据亚硫酸氢根离子和酸反应可以生成二氧化硫,检验二氧化硫完成实验设计,或通过亚硫酸氢根离子和氢氧化钡反应生成沉淀分析判断;实验设计方法和步骤为:
| 实验操作 | 预期现象与结论 |
| 步骤2:滴入1滴(或少量)品红,再滴入过量2mol/L盐酸,振荡 | 若品红褪色(或有气泡),则“吸收液”中存在SO32- 若品红不褪色(或无有气泡),则“吸收液”中不存在SO32- |
| 步骤3:用试管取适量滤液,向其中(或小烧杯中)滴入过量的1mol/L Ba(OH)2溶液[或滴入1滴(或少量)品红溶液,再滴入2-3滴(或过量)的2mol/L盐酸],振荡. | 若出现白色沉淀(或品红溶液褪色,或有气泡),则“吸收液”中存在HSO3-. 若不出现白色沉淀(或品红溶液不褪色,或没有气泡),则“吸收液”中不存在HSO3-. |
| 实验操作 | 预期现象与结论 |
| 步骤2:滴入1滴(或少量)品红,再滴入过量2mol/L盐酸,振荡 | 若品红褪色(或有气泡),则“吸收液”中存在SO32- 若品红不褪色(或无有气泡),则“吸收液”中不存在SO32- |
| 步骤3:用试管取适量滤液,向其中(或小烧杯中)滴入过量的1mol/L Ba(OH)2溶液[或滴入1滴(或少量)品红溶液,再滴入2-3滴(或过量)的2mol/L盐酸],振荡. | 若出现白色沉淀(或品红溶液褪色,或有气泡),则“吸收液”中存在HSO3-. 若不出现白色沉淀(或品红溶液不褪色,或没有气泡),则“吸收液”中不存在HSO3-. |

 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案[2012·广东肇庆市一模](14分)I:某兴趣小组欲在绿色环保的条件下探究大气污染物SO2的性质,设计如下图实验装置。请回答: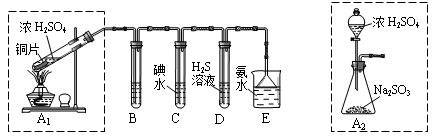
(1)B、C、D分别用于检验SO2的漂白性、还原性和氧化性,则B中所盛试剂为 ;
C中反应的离子方程式为 。
(2)为了实现绿色环保的目标,某同学设计了上图A2的制取装置来代替A1装置,与A1装置相比,A2装置的优点是 (写两点)。
II:用氨水吸收尾气中的SO2,“吸收液”中可能含有OH-、SO32-、SO42-、HSO3-等阴离子。请回答:
(3)氨水吸收过量SO2的反应的离子方程式为 。
(4)已知亚硫酸氢盐一般易溶于水,SO2也易溶于水。现有仪器和试剂为:小烧杯、试管、玻璃棒、胶头滴管、过滤装置和滤纸;2 mol/L盐酸、2 mol/LHNO3、1 mol/LBaCl2溶液、l mol/LBa(OH)2溶液、品红溶液、蒸馏水。请设计实验证明“吸收液”中存在SO32-、HSO3-,完成下表的实验操作、预期现象和结论:
| 实验操作 | 预期现象与结论 |
| 步骤1:取适量“吸收液”于小烧杯中,用胶头滴管取l mol/L BaCl2溶液向小烧杯滴加直至过量。 | 若出现白色浑浊,则溶液中存在SO32-或 SO42-。 |
| 步骤2:将小烧杯中的浊液过滤、洗涤,再用适量水把附在滤纸上的固体冲入另一小烧杯中;向冲下的固体 。 | 。 |
| 步骤3: 。 | 。 |
[2012·广东肇庆市一模](14分)I:某兴趣小组欲在绿色环保的条件下探究大气污染物SO2的性质,设计如下图实验装置。请回答:
(1)B、C、D分别用于检验SO2的漂白性、还原性和氧化性,则B中所盛试剂为 ;
C中反应的离子方程式为 。
(2)为了实现绿色环保的目标,某同学设计了上图A2的制取装置来代替A1装置,与A1装置相比,A2装置的优点是 (写两点)。
II:用氨水吸收尾气中的SO2,“吸收液”中可能含有OH-、SO32-、SO42-、HSO3-等阴离子。请回答:
(3)氨水吸收过量SO2的反应的离子方程式为 。
(4)已知亚硫酸氢盐一般易溶于水,SO2也易溶于水。现有仪器和试剂为:小烧杯、试管、玻璃棒、胶头滴管、过滤装置和滤纸;2 mol/L盐酸、2 mol/LHNO3、1 mol/LBaCl2溶液、l mol/LBa(OH)2溶液、品红溶液、蒸馏水。请设计实验证明“吸收液”中存在SO32-、HSO3-,完成下表的实验操作、预期现象和结论:
|
实验操作 |
预期现象与结论 |
|
步骤1:取适量“吸收液”于小烧杯中,用胶头滴管取l mol/L BaCl2溶液向小烧杯滴加直至过量。 |
若出现白色浑浊,则溶液中存在SO32-或 SO42-。 |
|
步骤2:将小烧杯中的浊液过滤、洗涤,再用适量水把附在滤纸上的固体冲入另一小烧杯中;向冲下的固体 。 |
。 |
|
步骤3: 。 |
。 |

 8SO2+2Fe2O3该反应中被氧化的元素是_______(填元素符号)。当该反应转移2.
75mol电子时,生成的二氧化硫在标准状况下的体积为_______L。
8SO2+2Fe2O3该反应中被氧化的元素是_______(填元素符号)。当该反应转移2.
75mol电子时,生成的二氧化硫在标准状况下的体积为_______L。