25℃时有关弱酸的电离平衡常数见下表:
|
【化学-化学与技术】某强酸性工业废水中含有Fe2+、Fe3+、Cu2+,设计实验方案用沉淀法除去铁离子,得到较纯的Cu2+溶液.有关氢氧化物沉淀的pH如下表:
(1)从表中数据分析,为什么不能直接加NaOH将溶液pH调到9.7来除去Fe3+和Fe2+ .
(2)实际应用中则是先加一定量的次氯酸钠,然后再调节溶液pH.次氯酸钠的作用是 .
(3)pH应调节到什么范围 ,为什么 .
(4)调节pH适宜的试剂是
A.氢氧化钡B.碳酸镁,C、氧化铜、D、稀盐酸
理由 .
0 21922 21930 21936 21940 21946 21948 21952 21958 21960 21966 21972 21976 21978 21982 21988 21990 21996 22000 22002 22006 22008 22012 22014 22016 22017 22018 22020 22021 22022 22024 22026 22030 22032 22036 22038 22042 22048 22050 22056 22060 22062 22066 22072 22078 22080 22086 22090 22092 22098 22102 22108 22116 203614
| 金属离子 | pH | |
| 开始沉淀 | 沉淀完全 | |
| Fe2+ | 6.3 | 9.7 |
| Cu2+ | 4.7 | 6.7 |
| Fe3+ | 1.9 | 3.2 |
(2)实际应用中则是先加一定量的次氯酸钠,然后再调节溶液pH.次氯酸钠的作用是
(3)pH应调节到什么范围
(4)调节pH适宜的试剂是
A.氢氧化钡B.碳酸镁,C、氧化铜、D、稀盐酸
理由

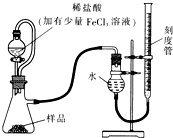 过氧化镁(MgO2)易溶于稀酸,溶于酸后产生过氧化氢,在医学上可作为解酸剂等.过氧化镁产品中常会混有少量MgO,实验室可通过多种方案测定样品中过氧化镁的含量.
过氧化镁(MgO2)易溶于稀酸,溶于酸后产生过氧化氢,在医学上可作为解酸剂等.过氧化镁产品中常会混有少量MgO,实验室可通过多种方案测定样品中过氧化镁的含量.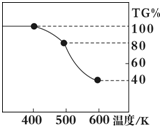 Ⅰ.某溶液中仅含如表离子中的5种离子(不考虑水的电离及离子的水解),且离子的物质的量均为1mol.
Ⅰ.某溶液中仅含如表离子中的5种离子(不考虑水的电离及离子的水解),且离子的物质的量均为1mol.