0 21566 21574 21580 21584 21590 21592 21596 21602 21604 21610 21616 21620 21622 21626 21632 21634 21640 21644 21646 21650 21652 21656 21658 21660 21661 21662 21664 21665 21666 21668 21670 21674 21676 21680 21682 21686 21692 21694 21700 21704 21706 21710 21716 21722 21724 21730 21734 21736 21742 21746 21752 21760 203614
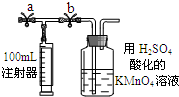 常温下甲醛是一种无色、有特殊刺激性气味的气体,易溶于水,是确定的致癌、致畸形物之一.我国规定:居室空气中甲醛的最高容许浓度为0.08mg/m3.某同学设计测定甲醛的方法如下(假设空气中无其它还原性气体):
常温下甲醛是一种无色、有特殊刺激性气味的气体,易溶于水,是确定的致癌、致畸形物之一.我国规定:居室空气中甲醛的最高容许浓度为0.08mg/m3.某同学设计测定甲醛的方法如下(假设空气中无其它还原性气体):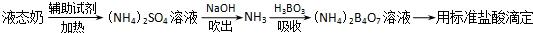
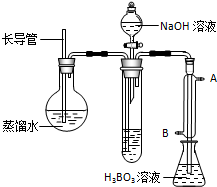
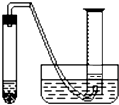 某学生拟通过测定粗锌(杂质与稀硫酸不反应)与稀硫酸反应产生的气体体积,来测定粗锌中锌的纯度.现有粗锌、稀硫酸、试管、镊子、单孔橡皮塞、导气管、托盘天平、量筒、水槽、铁架台(附铁夹)等仪器、药品.
某学生拟通过测定粗锌(杂质与稀硫酸不反应)与稀硫酸反应产生的气体体积,来测定粗锌中锌的纯度.现有粗锌、稀硫酸、试管、镊子、单孔橡皮塞、导气管、托盘天平、量筒、水槽、铁架台(附铁夹)等仪器、药品.

 中国青少年网络协会2005年11月在北京发布了我国首部《中国青少年网瘾数据报告》.报告指出,我国100个上网的青少年中有13个上网成瘾.有研究发现,在大脑的相应部位-“奖赏中心”,长时间上网会使“奖赏中心”的化学物质多巴胺水平升高,并认为,在各区域之间传递信息的化学物质是多巴胺,所以“奖赏中心”又称为多巴胺系统.多巴胺结构如图:
中国青少年网络协会2005年11月在北京发布了我国首部《中国青少年网瘾数据报告》.报告指出,我国100个上网的青少年中有13个上网成瘾.有研究发现,在大脑的相应部位-“奖赏中心”,长时间上网会使“奖赏中心”的化学物质多巴胺水平升高,并认为,在各区域之间传递信息的化学物质是多巴胺,所以“奖赏中心”又称为多巴胺系统.多巴胺结构如图: 可简写为
可简写为