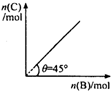
 在盛有足量 A 的体积可变的密闭容器中,加入 B,发生反应:A(s)+2B(g)=4C(g)+D(g);△H<0.在一定温度、压强下达到平衡.平衡时 C 的物质的量与加入的 B 的物质的量的变化关系如右图.下列说法正确的是( )
在盛有足量 A 的体积可变的密闭容器中,加入 B,发生反应:A(s)+2B(g)=4C(g)+D(g);△H<0.在一定温度、压强下达到平衡.平衡时 C 的物质的量与加入的 B 的物质的量的变化关系如右图.下列说法正确的是( )| A、平衡时 B 的转化率为 50% | B、若再加入 B,则再次达到平衡时正、逆反应速率均增大 | C、若保持压强一定,再加人 B,则反应体系气体密度减小 | D、若保持压强一定,当温度升高 10℃后,则图中 θ>45° |
 在盛有足量 A 的体积可变的密闭容器中,加入 B,发生反应:A(s)+2B(g)=4C(g)+D(g);△H<0.在一定温度、压强下达到平衡.平衡时 C 的物质的量与加入的 B 的物质的量的变化关系如右图.下列说法正确的是( )
在盛有足量 A 的体积可变的密闭容器中,加入 B,发生反应:A(s)+2B(g)=4C(g)+D(g);△H<0.在一定温度、压强下达到平衡.平衡时 C 的物质的量与加入的 B 的物质的量的变化关系如右图.下列说法正确的是( )| A、平衡时 B 的转化率为 50% | B、若再加入 B,则再次达到平衡时正、逆反应速率均增大 | C、若保持压强一定,再加人 B,则反应体系气体密度减小 | D、若保持压强一定,当温度升高 10℃后,则图中 θ>45° |