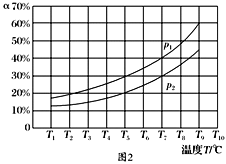
【题目】下列对有关微粒的相互关系和特征描述正确的是( )
选项 | 微粒 | 相互关系 | 特征描述 |
A | C60、C70、C540 | 同位素 | 微粒中只含非极性共价键 |
B | 新烷、2,2﹣二甲基丙烷 | 同分异构体 | 常温常压下呈气态 |
C |
| 同素异形体 | 铂作氨催化氧化时的催化剂 |
D | 甲酸、硬脂酸 | 同系物 | 能发生酯化反应 |
A. A B. B C. C D. D
【题目】电解质水溶液中存在电离平衡、水解平衡、溶解平衡,请回答下列问题。
(1)已知部分弱酸的电离常数如下表:
弱酸 | CH3COOH | HCN | H2CO3 |
电离常数(25℃) | Ka=1.8×10-5 | Ka=4.3×l0-10 | Ka1=5.0×l0-7 Ka2=5.6×l0-11 |
①0.1moI/LNaCN溶液和0.1mol/LNaHCO3溶液中,c(CN-)__c(HCO3-)(填“>”、“<”或“=”)。
②常温下,物质的量浓度相同的三种溶液:A.CH3COONa;B.NaCN;C.Na2CO3,其pH由大到小的顺序是___(填编号)。
③将少量CO2通入NaCN溶液,反应的离子方程式是__。
④室温下,-定浓度的CH3COONa溶液pH=9,用离子方程式表示溶液呈碱性的原因是__,溶液中![]() =__。(写出准确数值)
=__。(写出准确数值)
(2)某温度下,pH=3的盐酸中c(OH-)=10-9mol/L。该温度下,pH=2的H2SO4与pH=11的NaOH混合后pH变为9,则硫酸与氢氧化钠的体积比为__。
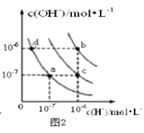
(3)室温下,用0.100mol/L盐酸溶液滴定20.00mL0.l00mol/L的某氨水溶液,滴定曲线如图所示(横坐标为盐酸的体积)。
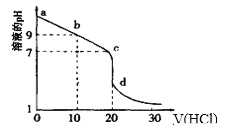
①d点所示的溶液中离子浓度由大到小的顺序依次为__。
②b点所示的溶液中c(NH4+)-c(NH3·H2O)=___。
(4)已知Ksp(BaSO4)=1.1×10-10,其溶解度为___g。(保留2位有效数字)
(5)室温下,已知Ksp(Fe(OH)3)=1×10-38,当Fe3+完全沉淀时,其溶液的pH=___。
【题目】新型储氢材料是开发利用氢能的重要研究方向。
(1)元素N的价电子数排布式为3d24s2,其氯化物NCl4和LiBH4反应可制得储氢材料N(BH4)3。
①元素N在周期表中的位置为__,该原子具有__种运动状态不同的电子。
②化合物LiBH4中含有的化学键有__,BH4-的立体构型是_,B原子的杂化轨道类型是__,B原子轨道表达式为__。
(2)金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径:Li+__H-(填“>”“=”或“<”)。
②某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:M的最高正价是__。
I1/kJ·mol-1 | I2/kJ·mol-1 | I3/kJ·mol-1 | I4/kJ·mol-1 | I5/kJ·mol-1 |
738 | 1451 | 7733 | 10540 | 13630 |
(3)NaH具有NaCl型晶体结构,Na+的配位数为__,晶体的堆积方式为__,已知NaH晶体的晶胞参数a=488pm,Na+半径为102pm,H-的半径为pm,NaH的理论密度是__g·cm-3。(仅写表达式,不计算)