��Ŀ����
����Ŀ�����ʹ�������ǿ����������ܵ���Ҫ�о�����
��1��Ԫ��N�ļ۵������Ų�ʽΪ3d24s2�����Ȼ���NCl4��LiBH4��Ӧ���Ƶô������N(BH4)3��
��Ԫ��N�����ڱ��е�λ��Ϊ__����ԭ�Ӿ���__���˶�״̬��ͬ�ĵ��ӡ�
�ڻ�����LiBH4�к��еĻ�ѧ����__��BH4-�����幹����_��Bԭ�ӵ��ӻ����������__��Bԭ�ӹ������ʽΪ__��
��2�������⻯���Ǿ������÷�չǰ���Ĵ�����ϡ�
��LiH�У����Ӱ뾶��Li��__H��(����������������������)��
��ij��������Ƕ����ڽ���Ԫ��M���⻯�M�IJ��ֵ��������±���ʾ��M�����������__��
I1/kJ��mol-1 | I2/kJ��mol-1 | I3/kJ��mol-1 | I4/kJ��mol-1 | I5/kJ��mol-1 |
738 | 1451 | 7733 | 10540 | 13630 |
��3��NaH����NaCl�;���ṹ��Na������λ��Ϊ__������Ķѻ���ʽΪ__����֪NaH����ľ�������a=488pm��Na���뾶Ϊ102pm��H���İ뾶Ϊpm��NaH�������ܶ���__g��cm-3��(��д����ʽ��������)
���𰸡��������ڵ���B�� 22 ���Ӽ������ۼ�����λ�� �������� sp3 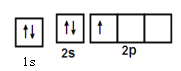 �� +2 6 �������ܶѻ�
�� +2 6 �������ܶѻ� ![]() g��(488��10��10cm)3
g��(488��10��10cm)3
��������
��1����Ԫ��N�ļ۵������Ų�ʽΪ3d24s2������Ԫ�أ�ԭ��������22��Ԫ��N�����ڱ��е�λ��Ϊ�������ڵ���B�壬Tiԭ�Ӻ�����22�����ӣ�������22�ֲ�ͬ�˶�״̬�ĵ��ӡ�
�ʴ�Ϊ���������ڵ���B�壻22��
��������LiBH4�У�Li+��BH4-���γ����Ӽ���B��H���γɹ��ۼ���������һ�����ۼ�����λ����LiBH4�к��еĻ�ѧ�������Ӽ������ۼ�����λ����
BH4����Bԭ�Ӽ۲������=4+![]() =4������Ϊsp3�ӻ����Ҳ����µ��Ӷԣ����������幹�ͣ�Bԭ�ӹ������ʽΪ
=4������Ϊsp3�ӻ����Ҳ����µ��Ӷԣ����������幹�ͣ�Bԭ�ӹ������ʽΪ ��
��
�ʴ�Ϊ�����Ӽ������ۼ�����λ�����������壻sp3 �� ��
��
��2�������Ӳ�ṹ��ͬ�����ӣ����Ӱ뾶����ԭ�������������С���������Ӱ뾶��Li����H�����ʴ�Ϊ������
����Ԫ�صĵ�III�����ܾ��������Ԫ�����ڵ�IIA�壬�������Ϊ+2���ʴ�Ϊ��+2��
��3��NaH����NaCl�;���ṹ����Na�������Cl-λ��Na�������¡�ǰ�����ң�Na������λ��Ϊ6������Ķѻ���ʽΪ�������ܶѻ���NaH����NaCl�;���ṹ��NaH����ľ�������a=488pm���ⳤ����Na���뾶Ϊ102pm��H���İ뾶Ϊ![]() =142pm���þ����������Ӹ���=8��
=142pm���þ����������Ӹ���=8��![]() +6��
+6��![]() =4�������Ӹ���=12��
=4�������Ӹ���=12��![]() +1=4��NaH�������ܶ�����=
+1=4��NaH�������ܶ�����= ==
==![]() g��(488��10��10cm)3=
g��(488��10��10cm)3=  g��cm-3=
g��cm-3= g��cm-3���ʴ�Ϊ��6���������ܶѻ���
g��cm-3���ʴ�Ϊ��6���������ܶѻ���![]() g��(488��10��10cm)3��
g��(488��10��10cm)3��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ�����ĵ��ʼ��仯�������ʶ�������;�㷺�����������գ�
��ѧ�������о����ô������������ٷɻ�β���е�NO��COת���CO2��N2��2NO+2CO![]() 2CO2+N2+Q(Q��0)��
2CO2+N2+Q(Q��0)��
��ij�¶��²�ø÷�Ӧ�ڲ�ͬʱ���COŨ�����±���
Ũ�ȣ�mol/L�� ʱ�䣨s�� | 0 | 1 | 2 | 3 | 4 | 5 |
c��CO�� | 3.60��10-3 | 3.05��10-3 | 2.85��10-3 | 2.75��10-3 | 2.70��10-3 | 2.70��10-3 |
��1���÷�Ӧƽ�ⳣ��K�ı���ʽΪ___���¶����ߣ�Kֵ___��ѡ��������������С��������������ǰ2s��ƽ����Ӧ����v��N2��=___�������߷�Ӧ���ܱ������з������ﵽƽ��ʱ�����NOת���ʵĴ�ʩ֮һ��___��
��2����ҵ�ϳɰ��ķ�Ӧ�¶�ѡ��500�����ҵ�ԭ����___��
��3��ʵ�����ڹ̶��ݻ����ܱ������м���1mol������3mol����ģ�ҵ�ϳɰ�����Ӧ��һ���������Ѵﵽƽ��ı�־��___��
A.N2��H2��NH3��Ũ��֮��Ϊ1��3��2
B.�����ڵ�ѹǿ���ֲ���
C.N2��H2��NH3��Ũ�Ȳ��ڱ仯
D.��Ӧֹͣ�������淴Ӧ�����ʶ�������
��4����������1molHCl��ϡ�����л���ͨ��1molNH3����Һ����仯���Բ��ƣ�����Ӧ��������Һ������Ũ���ɴ�С��˳����___����ͨ��NH3�Ĺ�������Һ�ĵ�������___��ѡ�������������С����������������
����Ŀ�����ж��й��������ϵ������������ȷ���ǣ� ��
ѡ�� | �� | ���ϵ | �������� |
A | C60��C70��C540 | ͬλ�� | ����ֻ���Ǽ��Թ��ۼ� |
B | ���顢2��2���������� | ͬ���칹�� | ���³�ѹ�³���̬ |
C |
| ͬ�������� | ������������ʱ�Ĵ��� |
D | ���ᡢӲ֬�� | ͬϵ�� | �ܷ���������Ӧ |
A. A B. B C. C D. D

