题目内容
【题目】下列中心原子的杂化轨道类型和分子几何构型不正确的是( )
A.PCl3中 P原子sp3杂化,为三角锥形
B.BCl3中B原子sp2杂化,为平面三角形
C.CS2中C原子sp杂化,为直线形
D.H2S中S原子sp杂化,为直线形
【答案】D
【解析】
A. 该分子中心原子的价层电子对数为![]() =4,孤电子对数为1,根据价层电子对互斥理论判断其中心原子杂化类型是sp3,实际空间构型为三角锥形,故A正确;
=4,孤电子对数为1,根据价层电子对互斥理论判断其中心原子杂化类型是sp3,实际空间构型为三角锥形,故A正确;
B.该离子中B原子价层电子对个数=![]() =3且不含孤电子对,根据价层电子对互斥理论判断B原子为sp2杂化,为平面三角形,故B正确;
=3且不含孤电子对,根据价层电子对互斥理论判断B原子为sp2杂化,为平面三角形,故B正确;
C.该分子中C原子价层电子对个数=![]() =2,且不含孤电子对,根据价层电子对互斥理论判断C原子采用sp杂化,为直线形结构,故C正确;
=2,且不含孤电子对,根据价层电子对互斥理论判断C原子采用sp杂化,为直线形结构,故C正确;
D.该分子中S原子价层电子对个数=![]() =4,且含有两对孤电子对,根据价层电子对判断S原子sp3杂化,分子构型为V形,故D错误;
=4,且含有两对孤电子对,根据价层电子对判断S原子sp3杂化,分子构型为V形,故D错误;
故选:D。

 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案【题目】下表列出了①~⑨九种元素在周期表中的位置:
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
1 | ① | |||||||
2 | ② | ③ | ④ | ⑧ | ||||
3 | ⑤ | ⑥ | ⑦ | ⑨ |
请按要求回答下列问题。
(1)元素④的名称是______,元素④在周期表中所处位置___________,从元素原子得失电子的角度看,元素④具有____________(填“氧化性”或“还原性”)。
(2)按气态氢化物的稳定性由弱到强的顺序排列,⑥④⑦的氢化物稳定性:_____________________(写氢化物的化学式)。
(3)元素⑦的原子结构示意图是____________。
(4)写出元素⑤形成的单质在氧气中燃烧的化学方程式________________,这一反应是___________(填“吸热”或“放热”)反应。
(5)用电子式表示①与⑨反应得到的化合物的形成过程_______________________。
【题目】亚硝酰氯(NOCl,熔点:-64.5℃,沸点:-5.5℃)是一种黄色气体,遇水易反应,生成一种氯化物和两种常见的氮氧化物,其中一种呈红棕色。可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。
(1)甲组的同学拟制备原料气NO和Cl2,制备装置如图所示:为制备纯净干燥的气体,下表中缺少的药品是:
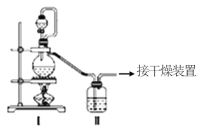
制备原料 | 装置Ⅰ | 装置Ⅱ | |
烧瓶中 | 分液漏斗中 | ||
制备纯净Cl2 | MnO2 | ①__ | 饱和食盐水 |
制备纯净NO | Cu | 稀硝酸 | ②__ |
(2)乙组同学利用甲组制得的NO和Cl2制备NOCl,装置如图所示:
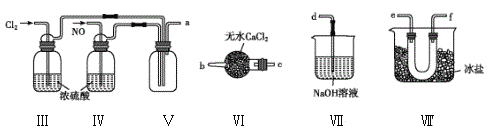
①装置连接顺序为a→____(按气流自左向右方向,用小写字母表示)。
②为了使气体充分反应,实验中先通入Cl2,待装置Ⅴ中充满黄绿色气体时,再将NO缓缓通入,此操作的目的是______(回答一条即可)。
③装置Ⅴ生成NOCl的化学方程式是________。
④装置Ⅵ的作用为___,若无该装置,Ⅷ中NOCl可能发生反应的化学方程式为__。
(3)丁组同学用以下方法测定亚硝酰氯(NOCl)纯度:
取Ⅷ中所得液体m克溶于水,配制成250mL溶液,取出25.00mL,以K2CrO4溶液为指示剂,用cmol/LAgNO3标准溶液滴定至终点,消耗标准溶液的体积为bmL。亚硝酰氯(NOCl)的质量分数为______(用代数式表示即可)。