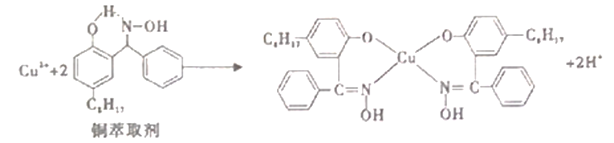
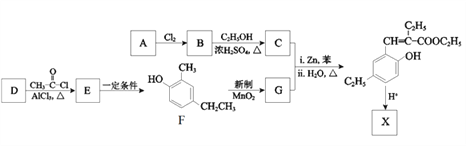
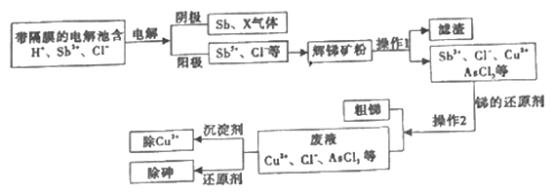
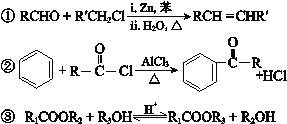【题目】环已酮是工业上的一种重要有机合成原料和溶剂.实验室制备原理为: ,其反应的装置示意图如下(夹持装置加热装置略去):
,其反应的装置示意图如下(夹持装置加热装置略去):
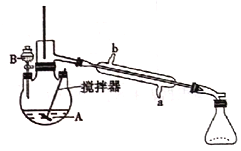
已知:
物质 | 沸点(℃) | 密度(g·cm-3,20℃) | 溶解性 |
环己醇 | 161.1(97.8) | 0.962 | 能溶于水 |
环已酮 | 155.6(95) | 0.948 | 微溶于水 |
(注:括号中的数据表示该有机物与水形成的具有固定组成的恒沸物的沸点)
(1)制备产品。通过仪器B____(填仪器名称)将酸性Na2Cr2O7和H2SO4混合溶被加到盛有环已醇的三颈烧瓶A中,通过______(填序号)方法加热到55-60℃进行反应。
a.酒精灯加热 b.油浴加热 c.水浴加热
(2)分离粗品。反应完成后,加入适量水,蒸馏,收集95-100℃的馏分(主要含环已酮粗品和水的混合物),试解释无法分离环己酮和水的原因是____________。
(3)提纯环已酮。
①在收集到的粗品中加NaCl固体至饱和,静置,分液。加入NaCl固体的作用是________。
②加入无水MgSO4固体,除去有机物中________ (填物质名称)。
③过滤,蒸馏,收集151-156℃馏分,得到精品。
(4)下列关于实验的叙述中,错误的是________。
A.冷凝管的冷水应该从b进从a出
B.实验开始时,温度计水银球应插入反应液中,便于控制反应液的温度
C.装置B中也可加入Na2Cr2O7和稀盐酸混合溶液
D.反应过程中,需不断搅拌
(5)利用环已酮做萃取剂可分离含Co2+、Mn2+的溶液,根据下图信息可判断,将pH范围控制在_______左右时可分离出Mn2+。

【题目】氮的固定有三种途径:生物固氮、自然固氮和工业固氮。根据最新“人工固氮”的研究报道:在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应,生成的主要产物为NH3。进一步研究NH3生成量与温度的关系,部分平衡时实验数据见下表(光照、N2压力1.0×105Pa、反应时间1 h):
T/K | 303 | 313 | 323 | 353 |
NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 | 2.0 |
相应的化学方程式:2N2(g)+6H2O(l)![]() 4NH3(g)+3O2(g) ΔH=a kJ·mol-1
4NH3(g)+3O2(g) ΔH=a kJ·mol-1
回答下列问题:
(1)此合成反应的a________0;(填“>”、“<”或“=”)
(2)从323 K到353 K,氨气的生成量减少的可能原因是_______________________________;(3)与目前广泛使用的工业合成氨方法相比,该方法固氮反应速率慢。请提出可提高其反应速率且增大NH3生成量的建议__________________________________________________。
(4)工业合成氨的反应为N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4 kJ·mol-1,分别研究在T1、T2和T3(T1<T2<T3)三种温度下合成氨气的规律。下图是上述三种温度下不同的H2和N2的起始组成比(起始时N2的物质的量均为1 mol)与N2平衡转化率的关系。请回答:
2NH3(g) ΔH=-92.4 kJ·mol-1,分别研究在T1、T2和T3(T1<T2<T3)三种温度下合成氨气的规律。下图是上述三种温度下不同的H2和N2的起始组成比(起始时N2的物质的量均为1 mol)与N2平衡转化率的关系。请回答:

①在上述三种温度中,曲线X对应的温度是________。
②a、b、c三点中H2的转化率最小的是_______点、转化率最大的是________点。
③在容积为1.0 L的密闭容器中充入0.30 mol N2(g)和0.80 molH2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为4/7。该条件下反应2NH3(g)![]() N2(g)+3H2(g)的平衡常数为__________________。
N2(g)+3H2(g)的平衡常数为__________________。
【题目】(1)工业上尝试用太阳能分解水制取H2,其过程如下:
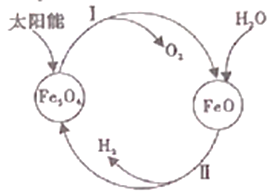
已知:2H2O(l)=2H2(g)+O2(g) △H=+571.6kJ/mol
2Fe3O4(s)![]() 6FeO(s)+O2(g) △H=+313.8kJ/mol
6FeO(s)+O2(g) △H=+313.8kJ/mol
①过程I中,需将O2及时分离出去,目的是_________。
②过程II的热化学方释式是_________。
③整个过程中,Fe3O4的作用是_________。
(2)工业上利用H2合成氢的反应原理为:3H2(g)+N2(g) ![]() 2NH3(g)。现有甲、乙两个容积为1L的密闭容器.在相同条件下,按不同的反应物投入量进行合成氢反应相关数据如下表示:
2NH3(g)。现有甲、乙两个容积为1L的密闭容器.在相同条件下,按不同的反应物投入量进行合成氢反应相关数据如下表示:
容器 | 甲 | 乙 |
反应物投入量 | 2molH2、2molN2 | 4malH2.4molN2 |
平衡时N2的浓度(mol/L) | c1=1.5 | c2 |
NH3的体积分数 | ω1 | ω2 |
混合气体的密度(g/L) | ρ1 | ρ2 |
①下列情况下,反应达到平衡状态的是_____(填序号)
a.3molH-H共价键断裂同时有6molN-H共价键形成
b.3v正(N2)=v逆(H2)
c.混合气体的平均相对分子质量保持不变
②反应的平衡常数K=_______(结果保留3位有效数字).
③分析上表中的数据,有以下关系:c2________3mol/L;ω1________ω2(填“>”、“<”、“=”);若ρ1=ag/L,则ρ2________g/L(用含a的式子表示)
(3)利用氨水吸收工业废气中的SO2,既可解决环境问题,又可制备(NH4)2SO3。可用(NH4)2SO3为原料,以空气氧化法制备(NH4)2SO4,其氧化速率与温度关系如下图:
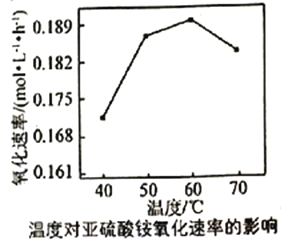
试解释在温度较高时,(NH4)2SO3氧化速率下降的原因是_________。