��Ŀ����
����Ŀ��ij�����Һ�п��ܺ���HCl��MgCl2��AlCl3��NH4Cl��Na2CO3��KCl�еļ������ʣ�������Һ����μ���NaOH��Һ���������������ʵ���(n)������NaOH��Һ���(V)�Ĺ�ϵ��ͼ��ʾ���ش��������⣺
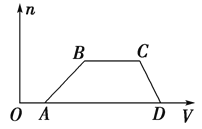
��1����Һ��һ�����е�������______________���ѧʽ����
��2����Һ��һ�������е�������____________���ѧʽ����
��3����Һ�п��ܺ��е�������__________�������ƣ����жϸ������Ƿ���ڵ�ʵ�鷽����________��������_____________��
��4���ֱ�д��AB�Ρ�BC�η��������ӷ���ʽ��
��AB��Ϊ________________________________��
��BC��Ϊ________________________________��
���𰸡���1��HCl��AlCl3��NH4Cl
��2��MgCl2��Na2CO3
��3���Ȼ��� ��ɫ��Ӧ ����ɫ�ܲ����۲���ɫ��Ӧ�Ƿ�Ϊ��ɫ
��4����Al3����3OH��===Al(OH)3�� ��NH4+��OH��=NH3��H2O
��������
���������OA����NaOH��Һ�к�HCl���������NaOH��Һ������ȫ���ܽ⣬˵����MgCl2�����Գ���ֻ��Al(OH)3��BC����NaOH��Һ��NH4Cl��Ӧ����ԭ��Һ��һ������HCl��AlCl3��NH4Cl��һ����MgCl2������ΪAlCl3��HCl��Na2CO3���ܴ������棬����һ����Na2CO3�����ܺ���KCl�� ������ɫ��Ӧ����ȷ������1����Һ��һ�����е�������HCl��AlCl3��NH4Cl��
��2����Һ��һ�������е�������MgCl2��Na2CO3��
��3����Һ�п��ܺ��е��������Ȼ������жϸ������Ƿ���ڵ�ʵ�鷽������ɫ��Ӧ������������ɫ�ܲ����۲���ɫ��Ӧ�Ƿ�Ϊ��ɫ��
��4��AB�Ρ�BC�η��������ӷ���ʽ����AB��ΪAl3����3OH��===Al(OH)3����
��BC��ΪNH4+��OH��=NH3��H2O��

����Ŀ���⡢������Ԫ����ɵij���������H2O��H2O2��������һ�������¾��ɷֽ⡣
��1����֪��
��ѧ�� | �Ͽ�1mol��ѧ�������������kJ�� |
H-H | 436 |
O-H | 463 |
O=O | 498 |
��H2O�ĵ���ʽ��________________��
��H2O(g)�ֽ���Ȼ�ѧ����ʽ��________________________��
��11.2 L����״������H2��ȫȼ�գ�������̬ˮ���ų�__________kJ��������
��2��ijͬѧ��H2O2�ֽ�Ϊ����̽��Ũ������Һ����ԶԷ�Ӧ���ʵ�Ӱ���������£����������ʾ�ķ������ʵ����
ʵ���� | ��Ӧ�� | ���� | |
a | 50 mL5%H2O2��Һ | 1 mL0.1 mol��L-1FeCl3��Һ | |
b | 50 mL5%H2O2��Һ | ����Ũ���� | 1 mL0.1 mol��L-1FeCl3��Һ |
c | 50 mL5%H2O2��Һ | ����ŨNaOH��Һ | 1 mL 0.1 mol��L-1FeCl3��Һ |
d | 50 mL5%H2O2��Һ | MnO2 | |
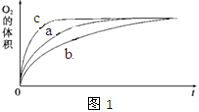
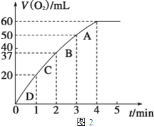
�� ���ʵ��a��b��c�����������������ʱ��仯�Ĺ�ϵ��ͼ1��ʾ���ɸ�ͼ�ܹ��ó���ʵ�������______________________��
�� ���ʵ��d�ڱ�״���·ų������������ʱ��仯�Ĺ�ϵ��ͼ2��ʾ�����ͷ�Ӧ���ʱ仯��ԭ��________________������H2O2�ij�ʼ���ʵ���Ũ��Ϊ________________ (������λ��Ч����)��