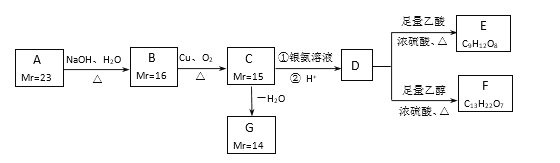
【题目】对于易燃、易爆、有毒的 化学物质,往往会在其包装上贴上危险警告标签.下面所 列的物质中,标签贴错了的是
选项 | A | B | C | D |
物质的化学式 | 氢氧化钠 | 金属汞 | 四氯化碳 | 烟花爆竹 |
危险警告标签 |
|
|
|
|
A. A B. B C. C D. D
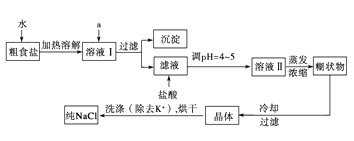
【题目】通过沉淀-氧化法处理含铬废水,减少废液排放对环境的污染,同时回收K2Cr2O7。实验室对含铬废液(含有Cr3+、Fe3+、K+、SO42-、NO3-和少量Cr2O72-)回收与再利用工艺如下:
已知:①Cr(OH)3+OH-=CrO2-+2H2O; ②2CrO2-+3H2O2+2OH-=2CrO42-+4H2O;M(Cr)=52
③H2O2在酸性条件下具有还原性,能将+6价Cr还原为+3价Cr。

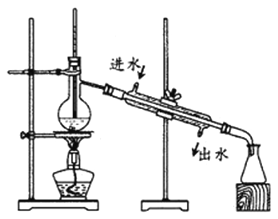
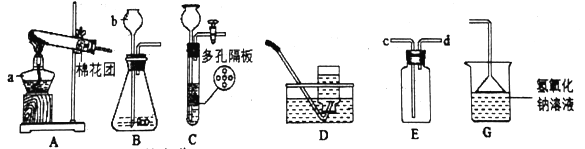
(1)抽滤过程中要及时观察吸滤瓶内液面高度,当快达到支管口位置时应进行的操作为_____________________________。
(2)滤液Ⅰ酸化前,进行加热的目的是____________________________;
冰浴、过滤后,应用少量冷水洗涤K2Cr2O7,其目的是________________________。
(3)下表是相关物质的溶解度数据:
物质 | 0℃ | 20℃ | 40℃ | 60℃ | 80℃ | 100℃ |
KCl | 28.0 | 34.2 | 40.1 | 45.8 | 51.3 | 56.3 |
K2SO4 | 7.4 | 11.1 | 14.8 | 18.2 | 21.4 | 24.1 |
K2Cr2O7 | 4.7 | 12.3 | 26.3 | 45.6 | 73.0 | 102.0 |
KNO3 | 13.9 | 31.6 | 61.3 | 106 | 167 | 246.0 |
根据溶解度数据,调节pH选择的试剂是__________________。
A.稀盐酸 B.稀硫酸 C.稀硝酸
操作Ⅰ具体操作步骤为①______________________、②____________________。
(4)称取产品重铬酸钾试样4.000g配成250mL溶液,取出25.00mL于锥形瓶中,加入10mL 2 mol·L-1H2SO4和足量碘化钠(铬的还原产物为Cr3+),放于暗处5min,然后加入100mL水,加入3mL淀粉指示剂,用0.2400 mol·L-1Na2S2O3标准溶液滴定(I2+2S2O32-=2I-+S4O62-)。
① 若实验中共用去Na2S2O3标准溶液30.00mL,所得产品的中重铬酸钾的纯度为__________________________(列式不计算,设整个过程中其它杂质不参与反应)。
② 若装Na2S2O3标准液的滴定管在滴定前有气泡滴定后没有气泡,测得的重铬酸钾的纯度将:______________________(填“偏高”、“偏低”、或“不变”)。