【题目】Ⅰ.(1)在2L定容密闭容器中通入1molN2(g)和3molH2(g),发生反应:
3H2(g)+N2(g)![]() 2NH3(g)△H<0,测得压强一时间图像如图甲,测得p2=0.6p1,此时温度与起始温度相同,在达到平衡前某一时刻(t1)若仅改变一种条件,得到如乙图像。
2NH3(g)△H<0,测得压强一时间图像如图甲,测得p2=0.6p1,此时温度与起始温度相同,在达到平衡前某一时刻(t1)若仅改变一种条件,得到如乙图像。
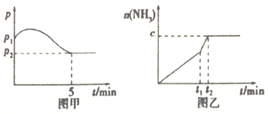
①若图中c=1.6mol,则改变的条件是__________(填字母,下同);
A.升温 B.降温 C.加压 D.减压 E.加催化剂
②若图中c<1.6mol,则改变的条件是__________(填字母);此时该反应的平衡常数__________(填“增大”、“减小”、“不变”)。
(2)如图甲,平衡时氢气的转化率为____________。
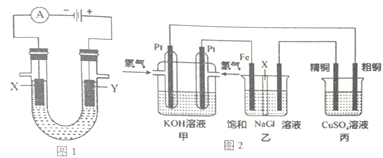
Ⅱ.粗制的CuCl2·2H2O晶体中常含有Fe3+、Fe2+杂质,为制得纯净的氯化铜晶体,首先将其制成水溶液,再按下图所示的操作步骤进行提纯。
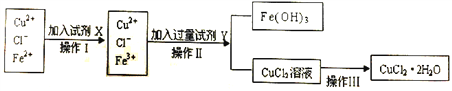
(1)操作Ⅰ时,常先加入合适的氧化剂,将Fe2+氧化为Fe3+,下列可选用的氧化剂是__________。
A.KMnO4 B.H2O2 C.Cl2 D.HNO3
(2)操作Ⅱ调整溶液的pH的Y试剂可选用下列中的__________。
A.NaOH(s) B.氨水 C.CuO(s) D.Cu(OH)2(s)
(3)已知溶度积常数如下表:
物质 | Cu(OH) | Fe(OH)2 | Fe(OH)3 |
Ksp | 2.2×10-20 | 8.0×10-16 | 4.0×10-38 |
将溶液的pH调至pH=4时,使Fe3+完全转化为Fe(OH)3沉淀而除去,此时c(Fe3+)=__________。
(4)若将CuCl2溶液蒸干后,再灼烧,得到的固体是__________(填化学式);操作Ⅲ后由CuCl2·2H2O晶体得到纯净无水CuCl2的合理操作是_____________________________________。
【题目】根据电离平衡常数(用Ka表示)的大小可以判断电解质的相对强弱。25℃时,有关物质的电离平衡常数如下表所示:
化学式 | HF | H2CO3 | HClO | H2SO3 |
电离平衡常数(Ka) | Ka=7.2×10-4 | Ka1=4.2×10-7 Ka2=5.6×10-11 | Ka=3.0×10-8 | Ka1=1.0×10-2 Ka2=5.0×10-8 |
(1)25℃时,同浓度的HF、H2CO3、HClO三种溶液中,pH最大的是____________(写化学式)。
(2)将0.1mol·L-1的HF溶液1mL加水稀释至10mL(假设温度不变),下列各量增大的是___________(填写字母)。
A.c(H+) B.c(H+)·c(OH-) C.c(H+)/c(HF) D.c(OH-)/c(H+)
(3)25℃时,现有物质的量浓度均为0.1mol·L-1的下列四种溶液:
①Na2CO3溶液 ②NaHCO3溶液 ③NaF溶液 ④NaClO溶液。
依据数据判断其pH由大到小的顺序是_________________________(填写序号)。
(4)根据H2SO3的电离平衡常数,计算25℃时,0.05mol·L-1Na2SO3溶液的pH=__________。
若某Na2SO3和NaHSO3的混合液呈中性,则溶液中c(SO32-)__________c(HSO3-)(填“大于”、“小于“或“等于")。