【题目】电解质的水溶液中存在电离平衡。
(1)醋酸是常见的弱酸。
①醋酸在水溶液中的电离方程式为______________。
②下列方法中,可以使醋酸稀溶液中CH3COOH电离程度增大的是______(填字母序号)。
a.滴加少量浓盐酸 b.微热溶液
c.加水稀释 d.加入少量醋酸钠晶体
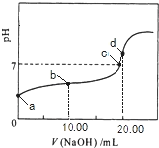
(2)用0.1mol/LNaOH溶液分别滴定体积均为20.00mL、浓度均为0.1mol/L的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线。

①滴定醋酸的曲线是_________(填“I”或“Ⅱ”)。
②滴定开始前,三种溶液中由水电离出的c(H+)最大的是_______。
③V1和V2的关系:V1___V2(填“>”、“=”或“<”)。
④M点对应的溶液中,各离子的物质的量浓度由大到小的顺序是_______。
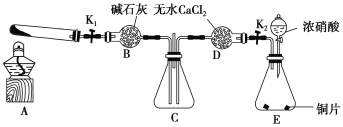
(3)为了研究沉淀溶解平衡和沉淀转化,某同学查阅资料并设计如下实验。
资料:AgSCN是白色沉淀,相同温度下,溶解度:AgSCN>AgI。
操作步骤 | 现象 |
步骤1:向2mL0.005mol/LAgNO3溶液中加入2mL0.005mol/L KSCN溶液,静置。 | 出现白色沉淀 |
步骤2:取1mL上层清液于试管中,滴加1滴2mol/LFe(NO3)3溶液。 | 溶液变红色。 |
步骤3:向步骤2的溶液中,继续加入5滴3mol/LAgNO3溶液。 | 现象a,溶液红色变浅。 |
步骤4:向步骤1余下的浊液中加入5滴3mol/LKI溶液。 | 出现黄色沉淀。 |
①写出步骤2中溶液变红色的离子方程式_____________。
②步骤3中现象a是_____________。
③用化学平衡原理解释步骤4的实验现象___________。
【题目】已知25℃时有关弱酸的电离平衡常数:
弱酸化学式 | HSCN | CH3COOH | HCN | H2CO3 |
电离平衡常数 | 1.3×10-1 | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7,K2=5.6×10-11 |
(1)等物质的量浓度的a.CH3COONa、b.NaCN、c.Na2CO3、d.NaHCO3溶液的pH由大到小的顺序为______________(填序号)。
(2)25℃时,将20mL0.1mol/LCH3COOH溶液和20mL0.1mol/LHSCN溶液分别与20mL0.1mol/LNaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如右图所示,反应初始阶段两种溶液产生CO2气体的速率存在明显差异的原因是________。反应结束后所得两溶液中,c(CH3COO-)____c(SCN-)(填“>”、“<”或“=")。

(3)若保持温度不变,在醋酸溶液中加少量盐酸,下列量会变小的是___(填序号)。
a.c(CH3COO-) b.c(H+) c.Kw d.醋酸电离平衡常数
【题目】室温下,将0.05 mol Na2CO3固体溶于水配成100mL溶液,向溶液中加入下列物质。有关结论正确的是
加入的物质 | 结论 | |
A | 50mL 1 mol/LH2SO4 | 反应结束后,c(Na+)=c(SO42-) |
B | 0.05molCaO | 溶液中c(OH-) /c(HCO3-) 增大 |
C | 50mL H2O | 由水电离出的c(H+)·c(OH—)不变 |
D | 0.1molNaHSO4固体 | 反应完全后,溶液pH减小,c(Na+)不变 |
A. A B. B C. C D. D
【题目】由煤制合成气(组成为H2、CO和CO2)制备甲醇或二甲醚是我国保障能源安全战略的重要措施。
(1)以澄清石灰水、无水硫酸铜、浓硫酸、灼热氧化铜为试剂检验合成气中含有H2、CO和CO2三种气体,所选用试剂及使用顺序为_______________________。
(2)制备甲醇(CH3OH)、二甲醚(CH3OCH3)主要过程包括以下四个反应:

①由H2 和CO可直接制备二甲醚:2CO(g)+ 4H2(g)==CH3OCH3(g)+H2O(g) ΔH=_____________。
分析上述反应(均可逆),二甲醚合成反应对于CO转化率的影响是_____________(填“增大”“ 减小”或“无影响”),其理由是______________________。
②有研究者用Cu -Zn –Al和Al2O3作催化剂。在压强为5.0Mpa的条件下,由合成气[![]() =2]直接副备二甲醚,结果如图所示。
=2]直接副备二甲醚,结果如图所示。

290℃时二甲醚的选择性(选择性=![]() ×100% 10)为97.8%,则290 ℃时二甲醚的产率为_______________________。
×100% 10)为97.8%,则290 ℃时二甲醚的产率为_______________________。
(3)在一个固定容积的密闭容器中,发生水煤气变换反应。
①下列各项能判断该反应已达到化学平衡状态的是________________(填字母)。
a.容器中压强不变 b. ΔH不变 c.V正(H2 )=v逆(CO) d.CO的质量分数不变
②温度为850℃时,该反应的平衡常数K=1,反应过程中各物质的浓度变化如下表:
时间/min | CO | H2O | CO2 | H2 |
0 | 0.200 | 0.300 | 0 | 0 |
2 | 0.138 | 0.238 | 0.062 | 0.062 |
3 | c1 | c2 | c3 | c4 |
4 | c1 | c2 | c3 | c4 |
5 | 0.065 | 0.21 | 0.125 |
0~4 min时,H2O(g)的转化率=______。表中4~5 min之间数值发生变化,可能的原因是___________
(填字母)。
a增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度