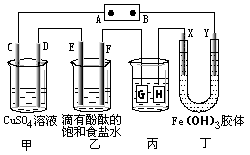
【题目】碘及其化合物在生产、生活中具有重要作用。请按要求回答下列问题:
(1)海带灰浸取液中的碘元素以I-形式存在。现利用如下试剂:MnO2、稀硫酸、淀粉溶液,从中获取单质碘。请按要求完善下表:
序号 | 所选试剂 | 反应原理或现象或解释 |
方法1 | MnO2、稀硫酸 | 离子方程式:________ |
方法2 | 稀硫酸、淀粉溶液 | 溶液变蓝的原因。用离子方程式解释: ____________ |
(2)反应2HI(g) ![]() H2(g)+I2(g)的能量变化如图1所示:其他条件相同,1molHI在不同温度分解达平衡时,测得体系中n(I2)随温度变化的曲线如图2所示。
H2(g)+I2(g)的能量变化如图1所示:其他条件相同,1molHI在不同温度分解达平衡时,测得体系中n(I2)随温度变化的曲线如图2所示。
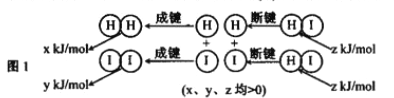

①比较2z______(x+y)(填 “<"、“>”或“=”).
②某温度下该反应的平衡常数K=1/9,达平衡时,HI的转化率=___________。
③只改变该反应的一个条件,试写出能提高HI转化率的两项措施:__________、_________。
(3)已知:i.分解1molH2O2放出热量98kJ;ⅱ.含少量I-的溶液中,H2O2的分解机为: H2O2+I-![]() H2O+IO-慢;H2O2+IO-
H2O+IO-慢;H2O2+IO-![]() H2O+O2+I-快。ⅲ.H2O2分解速率受多种因素影响,实验测得某温度时不同条件下H2O浓度随时间的变化如图3、4所示:
H2O+O2+I-快。ⅲ.H2O2分解速率受多种因素影响,实验测得某温度时不同条件下H2O浓度随时间的变化如图3、4所示:
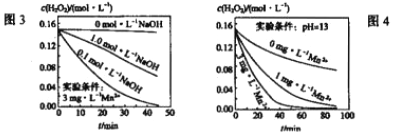
请完善由以上信息可得到的如下结论:
①H2O2分解反应的热化学方程式为___________。
②H2O2的分解速率与_________有关。
③“少量Mn2+存在时,溶液碱性越强H2O2分解速率越大”的结论是否正确_______(填“是"或“否”);c(Mn2+)对H2O分解速率的影响是__________。
【题目】研究CO2转化成有机物实现碳循环对实现社会的可持续发展具有重要的意义。将燃煤废气中的CO2转化为二甲醚的反应原理为2CO2(g)+6H2(g)![]() CH3OCH3(g)+3H2O(1)。
CH3OCH3(g)+3H2O(1)。
(1)已知一定压强下,该反应在温度升高时,CH3OCH3(g)的浓度减小,则反应的焓变△H_____0,熵变△S_______0(分别填“>”、“<”、或“=”)。
(2)相同条件下,在体积为2L的密闭容器内选用不同的催化剂,生成物二甲醚CH3OCH3的量随时间变化如图所示。

①图中0-4min内A的反应速率v(CO2)=________。该温度下平衡常数的表达式为________。
②下列有关说法正确的是______(填字母序号)。
A.反应的活化能大小顺序是:Ea(A)<Ea(B)< Ea(C)
B.升高温度能使反应速率加快,是因为活化分子百分数增大
C.单位时间内消耗CO2与生成H2的数目为3:1时,说明反应已经达到平衡
D.增大压强,平衡正向移动,平衡常数K值增大
(3)某温度下,在体积可变的密闭容器中,改变起始时各物质的起始投料量,在不同的压强下,平衡时生成物二甲醚CH3OCH3(g)的物质的量如下表所示:
序号 | 起始投料量不同的压强下, 平衡CH3OCH3(g)的量不同的压强 | P1 | P2 | P3 |
I | 2.0 molCO2 6.0molH2 | 0.10mol | 0.04 mol | 0.02mol |
II | 1.0molCO2 3.0molH2 | X1 | Y1 | Z1 |
III | 1.0mol CH3OCH3 3.0mol H2O | X2 | Y2 | Z2 |
①P1___P2(填“ >”、“<”或“=”);判断理由为____________。
②X1=______________。
③P2下,III中CH3OCH3的平衡转化率为_____________。