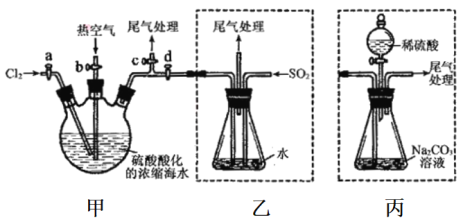
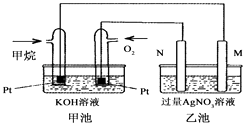
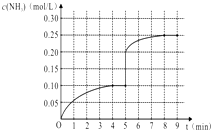
【题目】(I)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。当它们混合反应时,即产生大量氮气和水蒸气,并放出大量热。已知:0.4 mol液态肼与足量的液态双氧水反应,生成氮气和水蒸气,放出256.652 kJ的热量。
(1)该反应的热化学方程式为__________________________。
(2)下表是部分化学键的键能数据:
化学键 | P—P | P—O | O=O | P=O |
键能/(kJ/mol) | a | b | c | x |
已知白磷的燃烧热ΔH=-d kJ/mol,白磷及其完全燃烧的产物结构如下图所示,则上表中x=______________________(用含有a、b、c、d的代数式表示)。

(II)分别取40 mL的0.50 mol/L盐酸与0.55 mol/L氢氧化钠溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热。

请回答下列问题:
(3)A的仪器名称为_____________。
(4)如下图所示,泡沫塑料板上面有两个小孔,两个小孔不能开得过大,其原因是____________;反应需要测量温度,每次测量温度后都必须采取的操作是____________________。
(5)某学生实验记录数据如下:
实验序号 | 起始温度t1 ℃ | 终止温度t2 ℃ | |
盐酸 | 氢氧化钠 | 混合溶液 | |
1 | 20.0 | 20.1 | 23.2 |
2 | 20.2 | 20.4 | 23.4 |
3 | 20.5 | 20.6 | 23.6 |
已知盐酸和氢氧化钠溶液的密度都是1 g/cm3,又知中和后生成溶液的比热容c=4.18 J/(g·℃)
依据该学生的实验数据计算,该实验测得的中和热ΔH=________;
(6)假定该学生的操作完全同上,实验中改用100 mL 0.5 mol/L盐酸跟100 mL 0.55 mol/L氢氧化钠溶液进行反应,与上述实验相比,所放出的热量________(填“相等”或“不相等”),所求中和热________(填“相等”或“不相等”)。
【题目】碘及其化合物主要用于医药、照相及染料等。碘是合成碘化物的基本原料。
(一) 实验室测定KI溶液中I-的含量
量取25.00mLKI溶液溶液于250mL锥形瓶中,分别加入少量稀H2SO4和稍过量的NH4Fe(SO4)2·12H2O溶液,摇匀。小火加热蒸发至碘完全升华,取下锥形瓶冷却后,加入稀H2SO4,再加入几滴二苯胺磺酸钠(用作指示剂,被强氧化剂氧化为紫色),用0.0250mol·L-1标准K2Cr2O7溶液进行滴定至终点。重复3次,平均每次消耗K2Cr2O7溶液20.00mL(已知反应:①2Fe3++2I-=2Fe2++I2 ②6Fe2++Cr2O72-+14H+==6Fe3++2Cr3++7H2O
(1)在滴定过程中,下列操作(其他操作正确)会造成测定结果有误差的是_________________。
A.终点读数时俯视读数,滴定前平视读数
B.锥形瓶水洗后未干燥
C.滴定管未用标准K2Cr2O7溶液润洗
D.盛标准K2Cr2O7溶液的滴定管,滴定前有气泡,滴定后无气泡
(2)该实验达到滴定终点时,现象为__________________。
(3)根据滴定有关数据,该KI溶液中I-含量是________g·L-1。
(二) 某实验小组认为氧气可以氧化KI 溶液中的I-,其做了下列实验探究影响该反应的因素。
实验 | 气体a | 编号及现象 |
| 空气(含HCl) | Ⅰ.溶液迅速呈黄色 |
空气(含CO2) | Ⅱ.长时间后,溶液呈很浅的黄色 | |
空气 | Ⅲ.长时间后,溶液无明显变化 |
(4)装置A (含导管)的名称为_________________。
(5)通入a为空气(含HCl)时,发生反应的离子方程式为______________________。
(6)实验Ⅲ的作用是________________________。
(7)用CCl4萃取Ⅰ、Ⅱ、Ⅲ的溶液,萃取后下层溶液的颜色均无色。取萃取后上层溶液,用淀粉检验:Ⅰ、Ⅱ的溶液变蓝;Ⅲ的溶液未变蓝。溶液变蓝说明Ⅰ、Ⅱ中生成了__________________________。
(8)查阅资料: I2易溶于KI 溶液。下列实验证实了该结论并解释Ⅰ、Ⅱ的萃取现象。

现象X是_____。用KI萃取Ⅰ、Ⅱ的溶液,萃取后下层溶液颜色均无色的原因是_________________。
(9)综合实验证据说明影响I-被氧化的因素及对应关系:__________________________。
【题目】欲测定某NaOH溶液的物质的量浓度,可用0.1000molL﹣1的HCl标准溶液进行中和滴定(用甲基橙作指示剂).
请回答下列问题:
(1)滴定时,盛装待测NaOH溶液的仪器名称为 .
(2)盛装标准盐酸的仪器名称为 .
(3)滴定至终点的颜色变化为 .
(4)若甲学生在实验过程中,记录滴定前滴定管内液面读数为0.50mL,滴定后液面如图,则此时消耗标准溶液的体积为 . 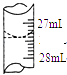
(5)乙学生做了三组平行实验,数据记录如下:
选取下述合理数据,计算出待测NaOH溶液的物质的量浓度为 (保留四位有效数字).
实验序号 | 待测NaOH溶液的体积/mL | 0.1000molL﹣1HCl溶液的体积/mL | |
滴定前刻度 | 滴定后刻度 | ||
① | 25.00 | 0.00 | 26.29 |
② | 25.00 | 1.00 | 31.00 |
③ | 25.00 | 1.00 | 27.31 |
(6)下列哪些操作会使测定结果偏高(填序号).
A.锥形瓶用蒸馏水洗净后再用待测液润洗
B.酸式滴定管用蒸馏水洗净后再用标准液润洗
C.滴定前酸式滴定管尖端气泡未排除,滴定后气泡消失
D.滴定前读数正确,滴定后俯视滴定管读数.