0 17932 17940 17946 17950 17956 17958 17962 17968 17970 17976 17982 17986 17988 17992 17998 18000 18006 18010 18012 18016 18018 18022 18024 18026 18027 18028 18030 18031 18032 18034 18036 18040 18042 18046 18048 18052 18058 18060 18066 18070 18072 18076 18082 18088 18090 18096 18100 18102 18108 18112 18118 18126 203614


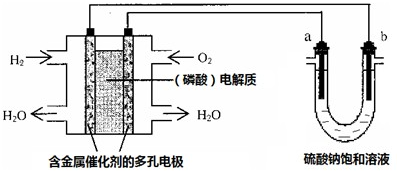
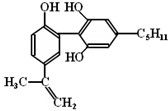 举办“人文奥运”的一个重要体现就是禁止运动员服用兴奋剂.有一种兴奋剂的结构简式如右式,下列有关该物质的说法正确的是( )
举办“人文奥运”的一个重要体现就是禁止运动员服用兴奋剂.有一种兴奋剂的结构简式如右式,下列有关该物质的说法正确的是( )