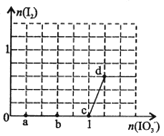
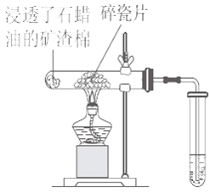
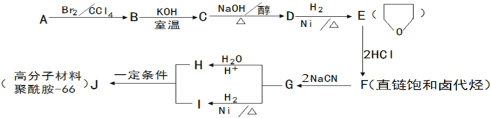
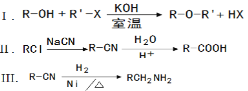
0 178048 178056 178062 178066 178072 178074 178078 178084 178086 178092 178098 178102 178104 178108 178114 178116 178122 178126 178128 178132 178134 178138 178140 178142 178143 178144 178146 178147 178148 178150 178152 178156 178158 178162 178164 178168 178174 178176 178182 178186 178188 178192 178198 178204 178206 178212 178216 178218 178224 178228 178234 178242 203614