甲醇是重要的化学工业基础原料和清洁液体燃料。工业上可利用CO或CO2来生产燃料甲醇。已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
化学反应 | 平衡常数 | 温度 | |
500 | 800 | ||
①2H2(g)+CO(g) | K1 | 2.5 | 0.15 |
②H2(g)+CO2(g) | K2 | 1.00 | 2.5 |
③3H2(g)+CO2(g) | K3 | ||
(1)在体积一定的密闭容器中发生反应②,达到平衡后升高温度,下列说法正确的是____________
A.平衡正向移动 B.达到新的平衡后体系的压强增大
C.H2的转化率增大 D.体系的密度增大
(2)某温度下反应①中H2的平衡转化率(α)与体系总压强(p)的关系如图所示,若开始加入2molH2和1molCO,A点时容器的体积为1L,则B点的化学平衡常数为_______。

(3)据反应①与②可推导出Kl、K2与K3之间的关系,则K3=__________。(用K1、K2表示)。500℃时测得反应③在某时刻,H2(g)、CO2(g)、CH3OH(g)、H2O(g) 的浓度(mol/L)分别为0.8、0.1、0.3、0.15,则此时v正_______ v逆(填“> ”、“= ”或“< ")。
(4)在3L容积可变的密闭容器中发生反应②,已知c(CO)一反应时间t变化曲线l如图所示,若在t0时刻分别改变一个条件,曲线I变为曲线II和曲线III。

当曲线I变为曲线II时,改变的条件可能是________。当曲线I变为曲线III时,改变的条件可能是___________。
(5)一定条件下甲醇与一氧化碳反应可以合成乙酸。通常状况下,将a mol/L的醋酸与bmol/LBa (OH)2溶液等体积混合,反应平衡时,2c(Ba2+)=c(CH3COO-),用含a和b的代数式表示该混合溶液中醋酸的电离常数为_______。
(1)N、Al、Si、Zn四种元素中,有一种元素的电离能数据如下:
电离能 | I1 | I2 | I3 | I4 | …… |
Ia(kJ/mol) | 578 | 1817 | 2745 | 11578 | …… |
则该元素是_______(填写元素符号)。
(2)基态C原子中,电子运动状态有_____种,电子占据的最高能级符号为_____,该能级含有的轨道数为________。
(3)关于化合物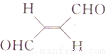 ,下列叙述正确的有______。
,下列叙述正确的有______。
A.分子间可形成氢键
B.分子中既有极性键又有非极性键
C.分子中有7个σ键和1个π键
D. C原子的杂化方式是sp2和sp3
(4)已知苯酚(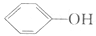 )具有弱酸性,其Ka=1.1×10-l0;水杨酸第一级电离形成的离子
)具有弱酸性,其Ka=1.1×10-l0;水杨酸第一级电离形成的离子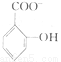 能形成分子内氢键。据此判断,相同温度下电离平衡常数Ka2(水杨酸)_____Ka(苯酚)(填“>”或“<”),其原因是____________。
能形成分子内氢键。据此判断,相同温度下电离平衡常数Ka2(水杨酸)_____Ka(苯酚)(填“>”或“<”),其原因是____________。
(5)在硅酸盐中,SiO44-四面体[如图(a)]通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根的一部分;Si与O的原子数之比为______,化学式为_______。

下列实验的现象以及结论均正确的是
选项 | 实验 | 现象 | 结论 |
A | 将少量的氯水滴入FeBr2溶液中,再滴 加CCl4振荡 | 下层溶液呈橙红色 | 还原性:Br->Fe2+ |
B | 向某无色溶液中滴加稀盐酸酸化的BaCl2溶液 | 产生白色沉淀 | 该溶液中一定存在SO42- |
C | 某钾盐溶于盐酸,将产生的无色无味气体通入澄清石灰水 | 石灰水变浑浊 | 该钾盐是K2CO3 |
D | 在两只试管中各加入2 mL5%H2O2浓溶液,向其中一只试管中滴入2滴0.1mol/LFeCl3溶液 | 加FeCl3溶液的试管中产生的气泡快 | 催化剂能增大化学反应速率 |
A. A B. B C. C D. D
 CH3OH(g)
CH3OH(g)



 在医药合成中有着广泛的用途。下列而关该物质的说法正确的是
在医药合成中有着广泛的用途。下列而关该物质的说法正确的是