10.设NA代表阿伏加德罗常数,下列说法中,正确的是( )
| A. | 2.3g金属钠全部变成钠离子时失去的电子数目为0.2NA | |
| B. | 2g氢气所含的原子数目为NA | |
| C. | 17gNH3所含的电子数为10NA | |
| D. | NA个氧分子和NA个氢分子的质量比等于16:1 |
9.可以用浓磷酸代替浓硫酸制取溴化氢气体的理由是( )
| A. | 浓磷酸与浓硫酸的性质相似 | |
| B. | 浓磷酸与浓硫酸一样难挥发,且属非氧化性酸 | |
| C. | 浓磷酸无氧化性,只有还原性 | |
| D. | 浓磷酸的酸性强于氢溴酸 |
8.0℃和1.01×105 Pa条件下,13g某气体与8g CH4的分子数目相同,则该气体在相应的条件下密度为( )
| A. | 0.36 g•L-1 | B. | 0.58 g•L-1 | C. | 1.16 g•L-1 | D. | 0.714 g•L-1 |
6.下列离子方程式书写正确的是( )
| A. | 铁跟稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 氧化镁与稀盐酸混合:O2-+2H+═2Cl--+H2O | |
| C. | 碳酸钙与稀盐酸反应:CO32-+2H+═CO2↑+H2O | |
| D. | 盐酸与澄清石灰水反应:H++OH-═H2O |
5.下列说法正确的是( )
| A. | 标况下22.4 L H2O和 1 mol O2所含分子数相等 | |
| B. | 1 mol水中含有2 mol氢和1 mol氧 | |
| C. | 1 mol气态水比1 mol液态水所含的分子数多 | |
| D. | 3 mol O2 与2 mol H2O所含原子数相等 |
4.已知醋酸达到电离平衡后,改变某条件电离平衡向正反应方向移动,则下列说法正确的是( )
| A. | 实现该变化的只能是升高温度 | B. | 溶液的导电能力一定变强 | ||
| C. | 溶液的pH一定减小 | D. | 发生电离的分子总数增多 |
2.下列说法或表示方法不正确的是( )
| A. | 盖斯定律实质上是能量守恒定律的体现 | |
| B. | 等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量更多 | |
| C. | 由C(石墨)→C(金刚石);△H=+73 kJ/mol,可知石墨比金刚石稳定 | |
| D. | 在稀溶液中:H+(aq)+OH-(aq)=H2O(l);△H=-57.3kJ/mol,若将含0.5mol H2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热量大于57.3kJ |
1.将20.9克由Cu、Al、Fe组成的合金溶于足量的NaOH溶液中,合金质量减少了2.7克.另取等质量的合金溶于过量的稀硝酸中,标准状况下生成了6.72LNO,向反应后的溶液中加入过量的NaOH溶液,则最终所得沉淀的质量为( )
0 173819 173827 173833 173837 173843 173845 173849 173855 173857 173863 173869 173873 173875 173879 173885 173887 173893 173897 173899 173903 173905 173909 173911 173913 173914 173915 173917 173918 173919 173921 173923 173927 173929 173933 173935 173939 173945 173947 173953 173957 173959 173963 173969 173975 173977 173983 173987 173989 173995 173999 174005 174013 203614
| A. | 28.4g | B. | 31.lg | C. | 27.2g | D. | 17.3g |
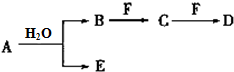 A、B、C、D、E、F为中学化学中的常见物质,且物质A由1~2种短周期元素组成,在一定条件下有如下转化关系,请完成下列问题:
A、B、C、D、E、F为中学化学中的常见物质,且物质A由1~2种短周期元素组成,在一定条件下有如下转化关系,请完成下列问题: ;D中所含化学键的类型离子键、共价键.
;D中所含化学键的类型离子键、共价键.