题目内容
3. A、B、C、D、E、F为中学化学中的常见物质,且物质A由1~2种短周期元素组成,在一定条件下有如下转化关系,请完成下列问题:
A、B、C、D、E、F为中学化学中的常见物质,且物质A由1~2种短周期元素组成,在一定条件下有如下转化关系,请完成下列问题:(1)若常温下A为有色气体.
①当F是一种金属单质时,请写出一定浓度的B溶液和足量F反应生成D与气体E的离子方程式:3Fe+8H++2NO3-=3Fe2++4H2O+2NO↑.
②当C是一种产生温室效应的气体分子时,E具有漂白性,物质F焰色反应呈黄色,则C的电子式为
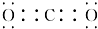 ;D中所含化学键的类型离子键、共价键.
;D中所含化学键的类型离子键、共价键.(2)若A为淡黄色固体,D为白色难溶于水的物质,且A和D的式量相等.
①用离子方程式表示F的水溶液呈酸性的原因Al3++3H2O?Al(OH)3+3H+.
②A可由对应的单质直接化合生成,生成39gA时,放出255.5kJ的热量,写出该反应的热化学方程式2Na (s)+O2(g)=Na2O2(s)△H=-551kJ•mol-1.
(3)若A中一种元素原子的最外层电子数为内层电子总数的1/5,将B和D分别溶于水,所得溶液按恰当比例混合,可得一种不含金属元素的盐溶液,请写出A与H2O反应的化学方程式:Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑;B与D反应生成无毒气体的化学方程式为8NH3+6NO2=7N2+12H2O.
分析 A、B、C、D、E、F为中学化学中的常见物质,且物质A由1~2种短周期元素组成,则B、E为短周期元素组成,
(1)①若F是一种金属单质,由转化关系可知,F为变价金属,应为Fe,B与Fe反应生成高价Fe,由于A为有色气体,与水反应生成B与E,则A为二氧化氮,B为硝酸、E为NO,C为硝酸铜、D为硝酸亚铁;
②C是一种产生温室效应的气体分子,则C为二氧化碳,E具有漂白性,物质F焰色反应呈黄色,则A为氯气、B为HCl、E为HClO,F为碳酸钠、D为碳酸氢钠,据此答题;
(2)A为淡黄色固体,能与水反应,则A为过氧化钠,物质A和D的式量相等,D为白色难溶于水的物质,结合转化关系,B为氢氧化钠、C为偏铝酸钠、F为铝盐、D为氢氧化铝、E为氧气;
(3)若物质A中一种元素原子的最外层电子数为内层电子总数的1/5,则该元素注意有3个电子层,最外层电子数为2,则该元素为Mg,B和D分别溶于水,所得溶液按恰当比例混合,可得一不含金属元素的盐溶液,为铵盐,A中含有氮元素,A为Mg3N2,结合转化关系,可知B为氨气、F为氧气、C为NO、D为硝酸,E为氢氧化镁.
解答 解:A、B、C、D、E、F为中学化学中的常见物质,且物质A由1~2种短周期元素组成,则B、E为短周期元素组成,
(1)①若F是一种金属单质,由转化关系可知,F为变价金属,应为Fe,B与Fe反应生成高价Fe,由于A为有色气体,与水反应生成B与E,则A为二氧化氮,B为硝酸、E为NO,C为硝酸铜、D为硝酸亚铁,一定浓度的B溶液和足量F反应生成D与气体E的离子方程式为:3Fe+8H++2NO3-=3Fe2++4H2O+2NO↑,
故答案为:3Fe+8H++2NO3-=3Fe2++4H2O+2NO↑;
②C是一种产生温室效应的气体分子,则C为二氧化碳,E具有漂白性,物质F焰色反应呈黄色,则A为氯气、B为HCl、E为HClO,F为碳酸钠、D为碳酸氢钠.二氧化碳的电子式为: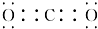 ,碳酸氢钠中含有离子键、共价键,
,碳酸氢钠中含有离子键、共价键,
故答案为: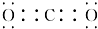 ;离子键、共价键;
;离子键、共价键;
(2)A为淡黄色固体,能与水反应,则A为过氧化钠,物质A和D的式量相等,结合转化关系,B为氢氧化钠、C为偏铝酸钠、F为铝盐、D为氧化铝、E为氧气.
①用离子方程式表示物质F的水溶液呈酸性的原因为:Al3++3H2O?Al(OH)3+3H+,
故答案为:Al3++3H2O?Al(OH)3+3H+;
②过氧化钠可由对应的单质直接化合生成,生成39g过氧化钠时,放出255.5kJ的热量,该反应的热化学方程式为2Na (s)+O2(g)=Na2O2(s)△H=-551kJ•mol-1,
故答案为:2Na (s)+O2(g)=Na2O2(s)△H=-551kJ•mol-1;
(3)若物质A中一种元素原子的最外层电子数为内层电子总数的1/5,则该元素注意有3个电子层,最外层电子数为2,则该元素为Mg,B和D分别溶于水,所得溶液按恰当比例混合,可得一不含金属元素的盐溶液,为铵盐,A中含有氮元素,A为Mg3N2,结合转化关系,可知B为氨气、F为氧气、C为NO、D为硝酸,E为氢氧化镁.A与H2O 反应的化学方程式为:Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑,B与D反应生成无毒气体为氮气,反应的化学方程式为:8NH3+6NO2=7N2+12H2O,
故答案为:Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑;8NH3+6NO2=7N2+12H2O.
点评 本题考查无机物推断,熟练掌握元素化合物的性质是关键,侧重考查学生对常见物质性质与特殊反应考查,难度中等.

 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案| A. | 第一电离能:Al>Mg | B. | 水溶性:CH3CH2OH>CH3CH2OCH2CH3 | ||
| C. | 沸点:HCl>HF | D. | 晶格能:NaCl>MgO |
| A. | 2:1 | B. | 78:31 | C. | 78:62 | D. | 39:62 |
| A. | 聚乙烯是通过加聚反应生成的 | |
| B. | 聚乙烯具有固定的元素组成,因而具有固定的熔、沸点 | |
| C. | 聚乙烯塑料袋因有毒,不可以装食品 | |
| D. | 聚乙烯因性质稳定,故不易造成污染 |
| A. | C2H6的结构简式:CH3CH3 | B. | O2-的结构示意图: | ||
| C. | CO2的结构式:O=C=O | D. | HClO的电子式:H:Cl:O: |
| A. | 0.36 g•L-1 | B. | 0.58 g•L-1 | C. | 1.16 g•L-1 | D. | 0.714 g•L-1 |
| A. | C3H4Cl2 | B. | CH4O | C. | C2H6O | D. | C2H4O2 |
| A. | I2 | B. | KIO3 | C. | HI | D. | KIO |
| A. | 阳离子只有氧化性,阴离子只有还原性 | |
| B. | 金属单质在反应中只能作还原剂,非金属单质在反应中只能作氧化剂 | |
| C. | 氧化剂在反应中失去电子,还原剂在反应中得到电子 | |
| D. | 氧化剂具有氧化性,还原剂具有还原性 |