20.上述三个反应中的物质中,能与稀硫酸发生氧化还原反应的是( )
| A. | O2 | B. | Fe(OH)2 | C. | Fe | D. | Fe(OH)3 |
19.下列氧化还原反应中电子转移情况分析正确的是( )
| A. |  | B. | 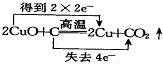 | ||
| C. |  | D. |  |
18.钠在坩埚中燃烧不可以证明的是( )
| A. | 钠的熔、沸点低 | |
| B. | 钠的颜色是银白色的 | |
| C. | 钠与空气中氧气反应,条件不同产物不同 | |
| D. | 因为反应要加热,所以该反应是吸热反应 |
17.只由两种元素组成的化合物,其中一种元素是氢元素,这类化合物称氢化物,如NaH.NaH是一种重要的生氢剂.它与水反应的方程式为:NaH+H2O═NaOH+H2↑.下面说法正确的是( )
| A. | NaH中H的化合价为-1价 | B. | H2O既不是氧化剂也不是还原剂 | ||
| C. | 该反应的离子方程式为:H-+H+═H2↑ | D. | NaOH是氧化产物 |
16.设NA为阿佛加德罗常数,下列对于0.3mol/L的K2SO4溶液的说法中正确的是( )
| A. | 溶液中含有0.6NA个K+ | |
| B. | 1L溶液中含有K+和SO42-总数为0.9NA | |
| C. | 取出10mL该溶液中,K+浓度为0.3mol/L | |
| D. | 100mL溶液中含有SO42-数目为0.6NA |
14.下列化学式表示的粒子对H2O的电离平衡不产生影响的是( )
| A. | 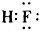 | B. | 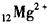 | C. |  | D. | OH- |
13.已知:酸性H2CO3>HClO>HCO${\;}_{3}^{-}$,判断在等浓度的NaClO、NaHCO3混合溶液中,各种离子浓度关系正确的是( )
| A. | c(Na+)>c(HCO${\;}_{3}^{-}$)>c(H+)>c(OH-) | |
| B. | c(HCO${\;}_{3}^{-}$)>c(ClO-)>c(OH-) | |
| C. | c(HClO)+c(ClO-)=c(HCO${\;}_{3}^{-}$)+c(H2CO3) | |
| D. | c(Na+)+c(H+)=c(HCO${\;}_{3}^{-}$)+c(ClO-)+c(OH-)+c(CO${\;}_{3}^{2-}$) |
12.下列热化学方程式中,正确的是( )
| A. | 甲烷的燃烧热△H=-890.3kJ/mol,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ/mol | |
| B. | 一定条件下,将0.5 mol N2和1.5 molH2置于密闭容器中充分反应生成NH3放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-38.6 kJ/mol | |
| C. | 在101kPa时,2gH2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ/mol | |
| D. | HCl和NaOH反应的中和热△H=-57.3 kJ/mol,则H2SO4和Ba(OH)2反应的中和热△H=2×(-57.3)kJ/mol |
11.下列化学式中,只表示一种纯净物的是( )
0 173808 173816 173822 173826 173832 173834 173838 173844 173846 173852 173858 173862 173864 173868 173874 173876 173882 173886 173888 173892 173894 173898 173900 173902 173903 173904 173906 173907 173908 173910 173912 173916 173918 173922 173924 173928 173934 173936 173942 173946 173948 173952 173958 173964 173966 173972 173976 173978 173984 173988 173994 174002 203614
| A. | C | B. | C3H8 | C. | C2H4O | D. | C3H6 |
 在lL的密闭容器中,充入1mol CO2和3mol H2,在500℃下发生反应CO2(g)+3H2(g)═CH3OH(g)+H2O(g),测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示:
在lL的密闭容器中,充入1mol CO2和3mol H2,在500℃下发生反应CO2(g)+3H2(g)═CH3OH(g)+H2O(g),测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示: