6.在相同的条件下,用下列两种方法制取氯气,①用含HCl 2mol的浓盐酸和足量的二氧化锰反应,②用43.5g 的MnO2和足量的浓盐酸反应,则所得Cl2 的物质的量( )
| A. | ①和②一样多 | B. | ②比①多 | C. | ①比②多 | D. | 无法比较 |
5.氯气是一种重要的工业原料.工业上利用下列反应来检查氯气管道是否漏气:
(1)3Cl2+2NH3═N2+6HCl (2)HCl+NH3═NH4Cl (氯化氢遇氨气产生白烟).下列说法错误的是
( )
(1)3Cl2+2NH3═N2+6HCl (2)HCl+NH3═NH4Cl (氯化氢遇氨气产生白烟).下列说法错误的是
( )
| A. | 反应(1)(2)中NH3都显还原性 | B. | 该反应中Cl2显强氧化性 | ||
| C. | 反应(1)属于置换反应 | D. | 生成2mol N2时转移12mol电子 |
4.在烧杯中加水和苯(密度为0.88g/cm3)各50mL.将一小粒金属钠(密度为0.97g/cm3)投入烧杯中,观察到的现象可能是( )
| A. | 钠在烧杯底部四处游动 | |
| B. | 钠停留在苯层中无气体放出 | |
| C. | 钠在苯的液面上反应并四处游动 | |
| D. | 钠在苯层与水层的交界处上下跳动,有气泡产生 |
3.能正确表示下列化学反应的离子方程式的是( )
| A. | 胆矾溶液和氢氧化钡溶液混合:2OH-+Cu2+═Cu(OH)2↓ | |
| B. | 澄清石灰水与稀盐酸反应:Ca(OH)2+2H+═Ca2++2H2O | |
| C. | 氯气通入氢氧化钠溶液中制84消毒液:Cl2+2OH -═Cl-+ClO-+H2O | |
| D. | 用醋酸除去热水瓶中的水垢(碳酸钙):CaCO3+2H+═Ca2++H2O+CO2↑ |
2.下列物质在水中的电离方程式正确的是( )
| A. | Na2CO3═Na2++CO32- | B. | NaHCO3═Na++HCO3- | ||
| C. | KClO3═K++Cl-+3O 2- | D. | H2SO4═H++SO42- |
1.对于某盐溶液中的离子检验及结论一定正确的是,取试样( )
| A. | 加入盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32- | |
| B. | 加入硝酸银溶液,生成白色沉淀,加稀盐酸沉淀不消失,一定有Cl- | |
| C. | 加入NaOH溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝,一定有NH4+ | |
| D. | 滴加BaCl2溶液,生成白色沉淀,再加入稀硝酸沉淀不溶,一定有SO42- |
17.研究CO2的利用对促进低碳社会的构建具有重要的意义.
(1)在一定体积的密闭容器中,进行化学反应:CO2(g)+H2(g)?CO(g)+H2O(g)
其化学平衡常数K和温度t的关系如表:
①该反应正向反应是吸热反应.(填“放热”或“吸热”)
②能判断该反应达到化学平衡状态的依据是BC.
A.容器压强不变 B.混合气体中c(CO2)不变
C.υ正(H2)=υ逆(H2O) D.c(CO2)=c(CO)
③当其他条件不变时,若缩小容器的体积,该反应平衡不移动.(选填“正向”、“逆向”或“不”)
(2)工业上合成甲醇可在密闭容器中采用如下反应进行:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1
①该反应的平衡常数表达式K=$\frac{c(CH{\;}_{3}OH)c(H{\;}_{2}O)}{c(CO{\;}_{2})c{\;}^{3}(H{\;}_{2})}$.
②某实验将1molCO2和3molH2充入一定体积的密闭容器中,在两种不同条件下发生反应(只有一种条件不同).测得CH3OH的物质的量随时间变化如图所示:

曲线I、Ⅱ对应的平衡常数大小关系为KⅠ>KⅡ(选填“>”、“=”或“<”).
③一定温度下,在容积2L且固定的两个密闭容器中,按如下方式加入反应物,一段时间后达到平衡.
经测定甲容器经过5min达到平衡,平衡时CO2的转化率为50%,甲容器中该反应在5min内的平均速率υ(H2)=0.15mol•L-1•min-1.
要使平衡后乙容器与甲容器中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则c的取值范围为0.5<n(c)<1.
0 173574 173582 173588 173592 173598 173600 173604 173610 173612 173618 173624 173628 173630 173634 173640 173642 173648 173652 173654 173658 173660 173664 173666 173668 173669 173670 173672 173673 173674 173676 173678 173682 173684 173688 173690 173694 173700 173702 173708 173712 173714 173718 173724 173730 173732 173738 173742 173744 173750 173754 173760 173768 203614
(1)在一定体积的密闭容器中,进行化学反应:CO2(g)+H2(g)?CO(g)+H2O(g)
其化学平衡常数K和温度t的关系如表:
| t/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
②能判断该反应达到化学平衡状态的依据是BC.
A.容器压强不变 B.混合气体中c(CO2)不变
C.υ正(H2)=υ逆(H2O) D.c(CO2)=c(CO)
③当其他条件不变时,若缩小容器的体积,该反应平衡不移动.(选填“正向”、“逆向”或“不”)
(2)工业上合成甲醇可在密闭容器中采用如下反应进行:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1
①该反应的平衡常数表达式K=$\frac{c(CH{\;}_{3}OH)c(H{\;}_{2}O)}{c(CO{\;}_{2})c{\;}^{3}(H{\;}_{2})}$.
②某实验将1molCO2和3molH2充入一定体积的密闭容器中,在两种不同条件下发生反应(只有一种条件不同).测得CH3OH的物质的量随时间变化如图所示:

曲线I、Ⅱ对应的平衡常数大小关系为KⅠ>KⅡ(选填“>”、“=”或“<”).
③一定温度下,在容积2L且固定的两个密闭容器中,按如下方式加入反应物,一段时间后达到平衡.
| 容器 | 甲 | 乙 |
| 反应物投入量 | 1molCO2、3molH2 | a molCO2、b molH2、 c molCH3OH(g)、c molH2O(g) |
要使平衡后乙容器与甲容器中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则c的取值范围为0.5<n(c)<1.
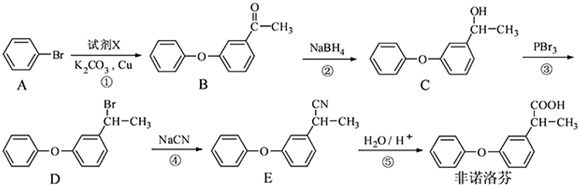
 .
. .
.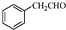 为原料制备
为原料制备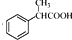 的合成路线流程图(无机试剂任用).
的合成路线流程图(无机试剂任用).