题目内容
19.(NH4)2SO4在高温下分解,产物是SO2、H2O、N2和NH3,写出发生反应的化学方程式:3(NH4)2SO4$\frac{\underline{\;高温\;}}{\;}$3SO2+6H2O+N2+4NH3↑.分析 硫酸铵受热分解生成SO2、H2O、N2和NH3,依据氧化还原反应得失电子守恒、原子个数守恒规律解答.
解答 解:由题意知;(NH4)2SO4在高温下分解产物是SO2、H2O、N2和NH3,属于氧化还原反应,铵根离子中-3价的N部分升高到0价,硫酸根离子中+6价的S化合价降低为二氧化硫中+4价S,依据得失电子守恒,氮气系数为1,则二氧化硫系数为3,依据原子个数守恒硫酸铵系数为3,氨气系数为4,水分子系数为6,化学方程式:3(NH4)2SO4$\frac{\underline{\;高温\;}}{\;}$3SO2+6H2O+N2+4NH3↑
故答案为:3(NH4)2SO4$\frac{\underline{\;高温\;}}{\;}$3SO2+6H2O+N2+4NH3↑.
点评 本题考查了化学方程式的书写,明确反应产物,氧化还原反应得失电子守恒、原子个数守恒是解题关键,题目难度不大.

练习册系列答案
相关题目
9.下列有关化学与生活、工业的叙述中正确的是( )
| A. | 漂粉精作消毒剂及铁粉作食品袋内的脱氧剂,它们均起还原作用 | |
| B. | 用明矾净水、用热碱水清除炊具上残留的油污、用浸泡过高锰酸钾溶液的硅藻土保鲜水果都涉及盐类的水解 | |
| C. | 硅胶、P2O5、六水氯化钙及具有吸水性的植物纤维均可作食品干燥剂 | |
| D. | 石墨烯弹性气凝胶制成的轻质“碳海绵”可用作处理海上原油泄漏的吸油材料 |
10.下列说法正确的是( )
| A. | NaOH固体溶于水后能导电,所以NaOH溶液是电解质 | |
| B. | H2SO4、Na2CO3、Ba(OH)2在水溶液中以离子的形式存在 | |
| C. | 液态氯化氢能导电,所以HCl是电解质 | |
| D. | NH3溶于水能导电,所以NH3是电解质 |
7.下列反应中水只做氧化剂的是( )
| A. | 2Na2O2+2H2O═4NaOH+O2↑ | B. | 3NO2+H2O═2HNO3+NO↑ | ||
| C. | NaH+H2O═NaOH+H2↑ | D. | 2F2+2H2O═4HF+O2↑ |
14.化学与生活、医疗密切相关.下列物质的俗名与化学式相对应的是( )
| A. | 天然气--CO | B. | 酒精--C2H5OH | C. | 金刚石--Si | D. | 石膏--CaCO3 |
4.在烧杯中加水和苯(密度为0.88g/cm3)各50mL.将一小粒金属钠(密度为0.97g/cm3)投入烧杯中,观察到的现象可能是( )
| A. | 钠在烧杯底部四处游动 | |
| B. | 钠停留在苯层中无气体放出 | |
| C. | 钠在苯的液面上反应并四处游动 | |
| D. | 钠在苯层与水层的交界处上下跳动,有气泡产生 |
11.设阿伏加德罗常数为NA,则下列说法正确的是( )
| A. | 甲烷的摩尔质量为16克 | |
| B. | 标准状况下,0.3molSO2中含氧原子数为0.3NA | |
| C. | 常温下,2.7克铝离子所带的电荷数为0.3NA | |
| D. | 常温下,9.5克MgCl2晶体中含Mg2+为0.2NA |
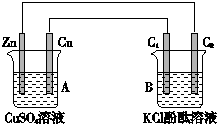 按图所示装置进行实验,并回答下列问题.
按图所示装置进行实验,并回答下列问题.