5.美国UNC化学教授Thomas J.Meyer等研发了环境友好、完全型的“绿色”引爆炸药,其中一种可表示为Na2R,它保存在水中可以失去活性,爆炸后不会产生危害性残留物.已知10mL Na2R溶液含Na+的数目为N,该Na2R溶液的物质的量浓度为( )
| A. | N×10-2mol•L-1 | B. | $\frac{N}{1.024×1{0}^{22}}$mol•L-1 | ||
| C. | $\frac{N}{6.02×1{0}^{21}}$mol•L-1 | D. | $\frac{N}{6.02×1{0}^{25}}$mol•L-1 |
3.在反应:2H2S+SO2═3S+2H2O中,当有4×6.02×1023个电子发生转移时,得到硫单质的物质的量为( )
| A. | 2mol | B. | 3mol | C. | 4mol | D. | 5mol |
2.下列物质中,按只有氧化性、只有还原性、既有氧化性又有还原性的顺序排列的一组是( )
| A. | Fe3+、K、Fe2+ | B. | Cl-、Al、H2 | C. | NO2、Na+、Br2 | D. | O2、SO2、Fe |
1.取100mL1.05mol•L-1的硫酸注入500mL容量瓶中,加水稀释至刻度线,该混合溶液中硫酸的物质的量浓度是( )
| A. | 0.21mol•L-1 | B. | 0.42mol•L-1 | C. | 0.56mol•L-1 | D. | 0.26mol•L-1 |
19.如图是某硫酸试剂瓶的标签上的部分信息.下列说法正确的是( )


| A. | 常温下,该试剂可与金属铝反应生成大量的无色气体 | |
| B. | 1mol Zn与足量的该硫酸反应生成2g氢气 | |
| C. | 该硫酸与等体积水混合所得溶液的物质的量浓度大于9.2mol/L | |
| D. | 向50mL该硫酸中加入足量的铜片,加热,反应后被还原的硫酸的物质的量等于0.46mol |
18.下列解释过程或事实的方程式不正确的是( )
| A. | 向Na2SO3、NaI的混合溶液中滴加少量氯水:2I-+C12═2Cl-+I2 | |
| B. | 熔融烧碱时,不能使用普通石英坩埚:SiO2+2NaOH$\frac{\underline{\;\;△\;\;}}{\;}$NaSiO3+H2O | |
| C. | 红热的铁丝与水接触,表面形成蓝黑色(或黑色)保护层:3Fe+4H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe3O4+4H2 | |
| D. | 漂白粉和“洁厕灵”(主要成分浓盐酸)混合使用放出氯气:ClO-+Cl-+2H+═Cl2↑+H2O |
17.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
0 173522 173530 173536 173540 173546 173548 173552 173558 173560 173566 173572 173576 173578 173582 173588 173590 173596 173600 173602 173606 173608 173612 173614 173616 173617 173618 173620 173621 173622 173624 173626 173630 173632 173636 173638 173642 173648 173650 173656 173660 173662 173666 173672 173678 173680 173686 173690 173692 173698 173702 173708 173716 203614
| A. | 标准状况下,22.4L CCl4含有4NA个共价键 | |
| B. | 1mol D2O所含的电子总数为12NA | |
| C. | 常温下,23g NO2含有NA个氧原子 | |
| D. | 1mol Fe2+与足量的H2O2溶液反应,转移2NA个电子 |
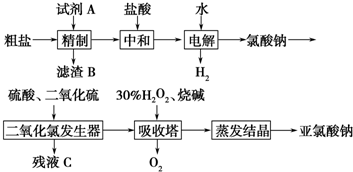
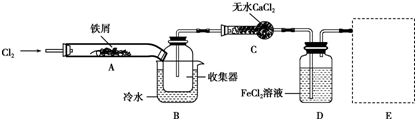
 .
.