题目内容
17.设NA为阿伏加德罗常数的数值,下列说法正确的是( )| A. | 标准状况下,22.4L CCl4含有4NA个共价键 | |
| B. | 1mol D2O所含的电子总数为12NA | |
| C. | 常温下,23g NO2含有NA个氧原子 | |
| D. | 1mol Fe2+与足量的H2O2溶液反应,转移2NA个电子 |
分析 A、标况下四氯化碳为液态;
B、重水中含10个电子;
C、求出二氧化氮的物质的量,然后根据1mol二氧化氮中含2mol氧原子来分析;
D、Fe2+与H2O2反应后变为+3价.
解答 解:A、标况下四氯化碳为液态,故不能根据气体摩尔体积来计算其物质的量和含有的共价键的个数,故A错误;
B、重水中含10个电子,故1mol重水中含10NA个电子,故B错误;
C、23g二氧化氮的物质的量为0.5mol,而1mol二氧化氮中含2mol氧原子,故0.5mol二氧化氮中含1mol氧原子即NA个,故C正确;
D、Fe2+与H2O2反应后变为+3价,故1mol亚铁离子转移1mol电子即NA个,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
7.下列叙述正确的是( )
| A. | 实验室可通过蒸馏的方法除去自来水中含有的氯离子等杂质制蒸馏水 | |
| B. | 将氢氧化钠稀溶液逐滴滴入氯化铁饱和溶液中,边滴边搅拌,可获得氢氧化铁胶体 | |
| C. | 由于氢氧化铁胶体带正电,所以电泳时阴极颜色加深 | |
| D. | 浓硫酸不慎溅到皮肤上,应该立即用大量水冲洗,然后涂上稀NaOH溶液 |
12.有A、B、C三种可溶性的盐,阴、阳离子各不相同,其阴离子的摩尔质量按A、B、C得顺序依次增大.将等物质的量的A、B、C溶于水,所得溶液中只含有Fe3+、K+、SO42-、NO3-、Cl-五种离子,同时生成一种白色沉淀AgCl,则A的化学式可能是( )
| A. | K2SO4 | B. | AgNO3 | C. | FeCl3 | D. | KCl |
2.下列物质中,按只有氧化性、只有还原性、既有氧化性又有还原性的顺序排列的一组是( )
| A. | Fe3+、K、Fe2+ | B. | Cl-、Al、H2 | C. | NO2、Na+、Br2 | D. | O2、SO2、Fe |
9.在一容积可变的密闭容器中,通入1mol X和3mol Y,在一定条件下发生如下反应:X(g)+3Y(g)?2Z(g),到达平衡后,Y的体积分数为a%,然后再向容器中通入2mol Z,保持在恒温恒压下反应,当达到新的平衡时,Y的体积分数为b%.则a与b的关系是( )
| A. | a=b | B. | a>b | C. | a<b | D. | 不能确定 |
6.下列关于胶体的叙述不正确的是( )
| A. | 胶体区别于其他分散系的本质特征是分散质的微粒直径在10-9~10-7m之间 | |
| B. | 胶体是一种均一、稳定的纯净物 | |
| C. | 用平行光照射CuSO4溶液和Fe(OH)3胶体时,产生的现象不相同 | |
| D. | Al(OH)3胶体能够吸附水中悬浮的固体颗粒沉降,达到净水目的 |
7.下列叙述中正确的是( )
| A. | 酸碱中和滴定时眼睛要注视着滴定管内液面的变化,以防止滴定过量 | |
| B. | 在海轮外壳上绑上锌块,可减缓外壳腐蚀,这是应用外加电流的阴极保护法来防腐 | |
| C. | 在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,则水分解的热化学方程式为:2H2O (l)═2H2(g)+O(g△H=571.6kJ/mol | |
| D. | 增大反应物浓度,使活化分子百分数增加,化学反应速率增大 |
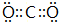 .
.