3.常温下,将0.1mol•L-1的醋酸溶液加水稀释至原来体积的10倍,下列有关叙述正确的是( )
| A. | CH3COOH的电离平衡常数增大为原来的10倍 | |
| B. | CH3COO-与CH3COOH的浓度之比增大为原来的10倍 | |
| C. | CH3COOH与CH3COO-的浓度之和减小为原来的$\frac{1}{10}$ | |
| D. | CH3COO-与H+的浓度之积减小为原来的$\frac{1}{10}$ |
2.部分弱酸的电离平衡常数如下表:
下列选项正确的是( )
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数 (25℃) | Ka=1.77×10-4 | Ka=4.9×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
| A. | 2CN-+H2O+CO2=2HCN+CO32- | |
| B. | 中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者大于后者 | |
| C. | 物质的量浓度相等的HCOONa和KCN溶液中,c(Na+)-c(HCOO-)<c(K+)-c(CN-) | |
| D. | c(NH4+) 相等的HCOONH4溶液、NH4CN溶液、NH4HCO3溶液中,c(NH4HCO3)>c(NH4CN)>c(HCOONH4) |
19.能正确表示下列过程的离子方程式是( )
| A. | S和热NaOH溶液的反应:4S+8NaOH═3Na2S+Na2SO4+4H2O | |
| B. | 除去CO2中的CO:2CO+O2═2CO2 | |
| C. | 向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+═2Fe(OH)3+3Mg2+ | |
| D. | 向漂白粉溶液中通入少量SO2气体:SO2+H2O+Ca2++ClO-═CaSO4+2H++Cl- |
18.已知:
①2CH3OH(g)=CH3OCH3(g)+H2O(g)△H1=-23.9kJ/mol
②2CH3OH(g)=C2H4(g)+2H2O(g)△H2=-29.1kJ/mol
③C2H5OH(g)=CH3OCH3(g)△H3=+50.7kJ/mol
则C2H4(g)+H2O(g)=C2H5OH(g)的是△H( )
①2CH3OH(g)=CH3OCH3(g)+H2O(g)△H1=-23.9kJ/mol
②2CH3OH(g)=C2H4(g)+2H2O(g)△H2=-29.1kJ/mol
③C2H5OH(g)=CH3OCH3(g)△H3=+50.7kJ/mol
则C2H4(g)+H2O(g)=C2H5OH(g)的是△H( )
| A. | -45.5kJ/mol | B. | +45.5kJ/mol | C. | -55.9kJ/mol | D. | +55.9kJ/mol |
16.下列对阿司匹林的描述错误的是( )
| A. | 化学名为乙酰水杨酸 | B. | 是一种难溶于水的白色晶体 | ||
| C. | 长期大量服用会出现不良反应 | D. | 是一种重要的抗生素即消炎药 |
15.下列各组的离子中,能在溶液中大量共存的是( )
0 173444 173452 173458 173462 173468 173470 173474 173480 173482 173488 173494 173498 173500 173504 173510 173512 173518 173522 173524 173528 173530 173534 173536 173538 173539 173540 173542 173543 173544 173546 173548 173552 173554 173558 173560 173564 173570 173572 173578 173582 173584 173588 173594 173600 173602 173608 173612 173614 173620 173624 173630 173638 203614
| A. | K+、H+、SO42-、OH- | B. | Na+、H+、Cl-、CO32- | ||
| C. | Na+、Ca2+、CO32-、NO3- | D. | K+、Cu2+、Cl-、SO42- |

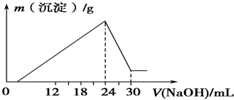
 Al(OH)3(胶体)+3H+.
Al(OH)3(胶体)+3H+.