1.热化学方程式S(l)+O2(g)═SO2(g);△H=-293.23kJ/mol.分析下列说法中不正确的是( )
| A. | S(s)+O2(g)═SO2(g),生成1mol SO2(g),反应放出的热量小于293.23 kJ | |
| B. | S(g)+O2(g)═SO2(g),生成1mol SO2(g),反应放出的热量大于293.23 kJ | |
| C. | 1 mol SO2的键能的总和大于1 mol 硫和1 mol 氧气的键能之和 | |
| D. | 1 mol SO2的键能的总和小于1 mol 硫和1 mol 氧气的键能之和 |
19.有序思维模式有利于解决复杂混合体系中的化学问题.下列反应先后顺序判断正确的是( )
| A. | 在含等物质的量的CO32-、OH-的溶液中逐滴加入稀盐酸:OH-、CO32-、HCO3- | |
| B. | 在含等物质的量的Al3+、NH4+的溶液中逐滴加入稀烧碱:Al3+、Al(OH)3、NH4+ | |
| C. | 在含铁和铜的混合物中逐滴加入稀硝酸:Fe、Cu、Fe2+ | |
| D. | 惰性电极电解含等物质的量的Zn2+、Al3+溶液时阴极电极反应:Zn2+、Al3+、H+ |
18.香草醛是一种食品添加剂,可由愈创木酚作原料合成,合成路线如图所示.下列说法正确的是( )


| A. | 在上述三步反应中理论上只有①生成②的反应原子利用率为100% | |
| B. | 氯化铁溶液和碳酸氢钠溶液都能鉴别①④ | |
| C. | ②③分子内含手性碳原子 | |
| D. | 在氢氧化钠溶液中,等物质的量的①和③分别消耗NaOH物质的量之比为1:2 |
16.食品添加剂关系到人类健康.下列物质中的添加剂作用不正确的是( )
| A. | 食盐加碘:着色剂 | B. | 火腿中的NaNO3:防腐剂 | ||
| C. | 炒菜放味精:调味剂 | D. | 用小苏打发面蒸馒头:膨松剂 |
15.能有效防止铁质栏杆锈蚀的措施是( )
| A. | 接上铜网 | B. | 与石墨相连 | C. | 定期涂上油漆 | D. | 定期擦去铁锈 |
14.新型柴油发动机的受热面由耐高温且不易传热的材料制造.这种材料最可能是( )
| A. | 陶瓷 | B. | 不锈钢 | C. | 纯铁 | D. | 铝合金 |
13. 某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.
某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.
Ⅰ.配制0.50mol/L NaOH溶液
(1)若实验中大约要使用245mL NaOH溶液,至少需要称量NaOH固体5.0g.
(2)配制0.50mol/L NaOH溶液必须用到的仪器有:天平(带砝码)、烧杯、玻璃棒、250ml容量瓶和胶头滴管.
Ⅱ.测定稀硫酸和稀氢氧化钠溶液中和热的实验装置如图所示.
(1)该图中有两处未画出,它们是烧杯上方的泡沫塑料盖和环形玻璃搅拌棒.泡沫塑料的作用是减少实验过程中的热量损失.
(2)写出该反应的热化学方程式(中和热△H=-57.3kJ/mol):$\frac{1}{2}$H2SO4(aq)+NaOH(aq)=$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-57.3kJ/mol
(3)取50mL NaOH溶液和30mL硫酸溶液进行实验,实验数据如表.
①请填写表中的空白:
②近似认为0.50mol/L NaOH溶液和0.50mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g•℃).则中和热△H=-53.5 kJ/mol (取小数点后一位).
③上述实验数值结果与-57.3kJ/mol有偏差,产生偏差的原因可能是(填字母)acd.
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度.
0 173335 173343 173349 173353 173359 173361 173365 173371 173373 173379 173385 173389 173391 173395 173401 173403 173409 173413 173415 173419 173421 173425 173427 173429 173430 173431 173433 173434 173435 173437 173439 173443 173445 173449 173451 173455 173461 173463 173469 173473 173475 173479 173485 173491 173493 173499 173503 173505 173511 173515 173521 173529 203614
 某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.
某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.Ⅰ.配制0.50mol/L NaOH溶液
(1)若实验中大约要使用245mL NaOH溶液,至少需要称量NaOH固体5.0g.
(2)配制0.50mol/L NaOH溶液必须用到的仪器有:天平(带砝码)、烧杯、玻璃棒、250ml容量瓶和胶头滴管.
Ⅱ.测定稀硫酸和稀氢氧化钠溶液中和热的实验装置如图所示.
(1)该图中有两处未画出,它们是烧杯上方的泡沫塑料盖和环形玻璃搅拌棒.泡沫塑料的作用是减少实验过程中的热量损失.
(2)写出该反应的热化学方程式(中和热△H=-57.3kJ/mol):$\frac{1}{2}$H2SO4(aq)+NaOH(aq)=$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-57.3kJ/mol
(3)取50mL NaOH溶液和30mL硫酸溶液进行实验,实验数据如表.
①请填写表中的空白:
| 实验次数] | 起始温度t1/°C] | 终止温度t2/°C] | 温度差平均值(t2-t1)/°C] | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | |
| 2 | 27.0 | 27.4 | 27.2 | 31.2 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
③上述实验数值结果与-57.3kJ/mol有偏差,产生偏差的原因可能是(填字母)acd.
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度.
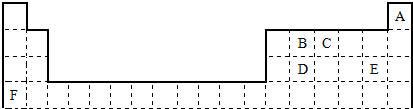
 .比较E、F的两种简单离子的半径大小:E-大于(填大于或小于)F+
.比较E、F的两种简单离子的半径大小:E-大于(填大于或小于)F+ A、B、C、D、E、F六种物质的相互转化关系如右图所示.图中反应条件均未标出,部分产物(包括水)已略去,反应①是置换反应.
A、B、C、D、E、F六种物质的相互转化关系如右图所示.图中反应条件均未标出,部分产物(包括水)已略去,反应①是置换反应. 如图所示,在一烧杯中盛有NaHSO4溶液,同时有一表面光滑的塑料小球悬浮于溶液中央.向该烧杯里缓缓注入Ba(OH)2溶液至Ba(OH)2过量.试回答:
如图所示,在一烧杯中盛有NaHSO4溶液,同时有一表面光滑的塑料小球悬浮于溶液中央.向该烧杯里缓缓注入Ba(OH)2溶液至Ba(OH)2过量.试回答: