2.PbO2受热分解为Pb的+4和+2价的混合氧化物,+4价的Pb能氧化浓盐酸生成Cl2;现将1mol PbO2加热分解得到O2,向剩余固体中加入足量的浓盐酸得到Cl2,O2和Cl2的物质的量之比为1:1,则剩余固体的组成及物质的量比可能是( )
| A. | 1:2:1混合的PbO2、Pb3O4、PbO | B. | 1:3:2混合的PbO2、Pb3O4、PbO | ||
| C. | 1:1:1混合的PbO2、Pb3O4、PbO | D. | 2:1:1混合的PbO2、Pb3O4、PbO |
1.关于下列四个图象的说法正确的是( )

| A. | 已知图①是体系Fe3+(aq)+SCN-(aq)?Fe(SCN)2+(aq) 中的c[Fe(SCN)2+]温度T的平衡图象.A点与B点相比,A点的c(Fe3+) 大 | |
| B. | 图②表示镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积V 与时间t的关系.则反应中镁和铝的反应速率之比为2:3 | |
| C. | 图③表示电源X极为正极,U形管中为AgNO3溶液,则b管中电极反应式是:4OH--4e-=O2↑+2H2O | |
| D. | 图④表示分离CCl4萃取碘水后已分层的有机层和水层 |
20.NA代表阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 1.0 L 1.0 mo1•L-1的NaAlO2 水溶液中含有的氧原子数为2 NA | |
| B. | 密闭容器中2 mol NO与1 mol O2充分反应,产物的分子数为2 NA | |
| C. | 过氧化钠与水反应时,生成0.1 mol 氧气转移的电子数为0.2 NA | |
| D. | 标准状况下,33.6 L氟化氢中含有氟原子的数目为1.5 NA |
19.化学在生产和日常生活中有着重要的应用.下列说法不正确的是( )
| A. | 明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 | |
| B. | 在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 | |
| C. | 根据是否具有丁达尔效应,将分散系分为溶液、浊液、胶体 | |
| D. | 工业上电解熔融的MgCl2,可制得金属镁 |
18.(1)恒温、容积为1L恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图1所示[已知:2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ/mol].

请回答下列问题:
①写出能表示硫的燃烧热的热化学方程式:S(s)+O2(g)═SO2(g)△H=-297 KJ•mol-1.
②△H2=-78.64 kJ/mol.
③在相同条件下,充入1mol SO3和0.5mol O2,则达到平衡时SO3的转化率为20%;此时该反应吸收(填“放出”或“吸收”)19.66 kJ的能量.
(2)中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%.①有效“减碳”的手段之一是节能,下列制氢方法最节能的是C(填序号).
A.电解水制氢:2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑
B.高温使水分解制氢:2H2O(g)$\frac{\underline{\;高温\;}}{\;}$2H2+O2↑
C.太阳光催化分解水制氢:2H2O $\frac{\underline{\;\;\;TiO_{2}\;\;\;}}{太阳光}$2H2↑+O2↑
D.天然气制氢:CH4+H2O(g) $\stackrel{高温}{?}$CO+3H2
②CO2可转化成有机物实现碳循环.在体积为1L的密闭容器中,充入1mol CO2和3mol H2,一定条件下反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol,测得CO2和CH3OH(g)浓度随时间变化如图2所示.
从3min到9min,υ(H2)=0.125 mol/(L•min).
③能说明上述反应达到平衡状态的是D(填编号).
A.反应中CO2与CH3OH的物质的量浓度之比为1:1(即图中交叉点)
B.混合气体的密度不随时间的变化而变化
C.3个H-H键断裂的同时有4个C-H键断裂
D.CO2的体积分数在混合气体中保持不变
(3)工业上,CH3OH也可由CO和H2合成.参考合成反应CO(g)+2H2(g)?CH3OH(g)的平衡常数.
下列说法正确的是AB.
A.该可逆反应的正反应是放热反应
B.在T℃时,1L密闭容器中,投入0.1molCO和0.2molH2,达到平衡时,CO的转化率为50%,则此时的平衡常数为100
C.工业上采用稍高的压强(5MPa)和250℃,是因为此条件下,原料气的转化率最高.

请回答下列问题:
①写出能表示硫的燃烧热的热化学方程式:S(s)+O2(g)═SO2(g)△H=-297 KJ•mol-1.
②△H2=-78.64 kJ/mol.
③在相同条件下,充入1mol SO3和0.5mol O2,则达到平衡时SO3的转化率为20%;此时该反应吸收(填“放出”或“吸收”)19.66 kJ的能量.
(2)中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%.①有效“减碳”的手段之一是节能,下列制氢方法最节能的是C(填序号).
A.电解水制氢:2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑
B.高温使水分解制氢:2H2O(g)$\frac{\underline{\;高温\;}}{\;}$2H2+O2↑
C.太阳光催化分解水制氢:2H2O $\frac{\underline{\;\;\;TiO_{2}\;\;\;}}{太阳光}$2H2↑+O2↑
D.天然气制氢:CH4+H2O(g) $\stackrel{高温}{?}$CO+3H2
②CO2可转化成有机物实现碳循环.在体积为1L的密闭容器中,充入1mol CO2和3mol H2,一定条件下反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol,测得CO2和CH3OH(g)浓度随时间变化如图2所示.
从3min到9min,υ(H2)=0.125 mol/(L•min).
③能说明上述反应达到平衡状态的是D(填编号).
A.反应中CO2与CH3OH的物质的量浓度之比为1:1(即图中交叉点)
B.混合气体的密度不随时间的变化而变化
C.3个H-H键断裂的同时有4个C-H键断裂
D.CO2的体积分数在混合气体中保持不变
(3)工业上,CH3OH也可由CO和H2合成.参考合成反应CO(g)+2H2(g)?CH3OH(g)的平衡常数.
| 温度/℃ | 0 | 100 | 200 | 300 | 400 |
| 平衡常数 | 667 | 13 | 1.9×10-2 | 2.4×10-4 | 1×10-5 |
A.该可逆反应的正反应是放热反应
B.在T℃时,1L密闭容器中,投入0.1molCO和0.2molH2,达到平衡时,CO的转化率为50%,则此时的平衡常数为100
C.工业上采用稍高的压强(5MPa)和250℃,是因为此条件下,原料气的转化率最高.
17.在密闭容器中,xA(g)+yB(g)?zC(g)反应达平衡时,A的浓度为0.5mol/L.若保持温度不变,将容器的容积扩大到原来的2倍,达新平衡时A的浓度降为0.3mol/L,则下列判断正确的是( )
| A. | x+y<z | B. | 平衡向正反应方向移动 | ||
| C. | B 的转化率增加 | D. | C 的体积分数下降 |
16.下列关于反应能量的说法正确的是( )
| A. | Zn(s)+CuSO4(aq)═ZnSO4(aq)+Cu(s)△H=-216 kJ•mol-1,则反应物总能量大于生成物总能量 | |
| B. | 若一定条件下,A═B△H<0,说明A物质比B物质稳定 | |
| C. | 101 kPa时,2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ•mol-1,则H2的燃烧热为571.6 kJ•mol-1 | |
| D. | H+ (aq)+OH- (aq)═H2O(l)△H=-57.3 kJ•mol-1,含1 mol NaOH的溶液与含0.5 mol H2SO4的浓硫酸混合后放出57.3 kJ的热量 |
14.下列叙述正确的是( )
0 172327 172335 172341 172345 172351 172353 172357 172363 172365 172371 172377 172381 172383 172387 172393 172395 172401 172405 172407 172411 172413 172417 172419 172421 172422 172423 172425 172426 172427 172429 172431 172435 172437 172441 172443 172447 172453 172455 172461 172465 172467 172471 172477 172483 172485 172491 172495 172497 172503 172507 172513 172521 203614
| A. | 稀醋酸中加入少量醋酸钠固体能增大醋酸的电离程度 | |
| B. | 25℃时,等体积等浓度的硝酸与氨水混合后,溶液呈中性 | |
| C. | 25℃时,0.1mol•L-1的硫化氢溶液比等浓度的硫化钠溶液的导电能力弱 | |
| D. | FeCl3和MnO2均可加快H2O2分解,同等条件下二者对H2O2分解速率的改变相同 |
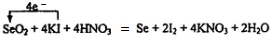 .
.