1.有关碱金属的叙述正确的是( )
| A. | 随核电荷数的增加,碱金属单质的熔点逐渐降低,密度逐渐增大 | |
| B. | 碱金属单质的金属性很强,均易与氯气、氧气、氮气等发生反应 | |
| C. | 碳酸铯加热时不能分解为二氧化碳和氧化铯 | |
| D. | 无水硫酸铯的化学式为Cs2SO4,它不易溶于水 |
20.下列文字表述与反应方程式对应且正确的是 ( )
| A. | 0.5mol/LNaHSO4与0.5mol/LBa(OH)2混合至溶液呈中性:Ba2++OH-+SO42-+H+═BaSO4↓+H2O | |
| B. | 向2mol/LFe(NO3)2(aq)中滴加少量氢碘酸:3Fe2++NO3-+4H+═3Fe3++NO↑+2H2O | |
| C. | 向20mL0.5mol/LFeBr2(aq)中通入224mLCl2(标况):2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- | |
| D. | 向30mL0.5mol/LNaOH(aq)中通入224mLCO2(标况):3OH-+2CO2═CO32-+HCO3-+H2O |
19.下列反应的离子方程式正确的是( )
| A. | NaAlO2溶液中滴加NaHCO3溶液:AlO2-+HCO3-+H2O═Al(OH)3↓+CO32- | |
| B. | 碘水中通入适量的SO2:I2+SO2+2H2O═2HI+SO42-+2H+ | |
| C. | FeSO4溶液中滴加双氧水:2Fe2++2H2O2═2Fe3++O2↑+2H2O | |
| D. | 向Ca(ClO)2溶液中通入足量SO2:ClO-+H2O+SO2═HClO+HSO3- |
17.某实验小组用0.50mol/LNaOH溶液和0.50mol/L溶液进行中和热的测定.通过测定反应过程中所放出的热量可计算中和反应热.回答下列问题:

(1)从实验装置上看,图中尚缺少的一种玻璃仪器是环形玻璃搅拌棒.
(2)大烧杯上如不盖硬纸板,求得的中和反应热数值偏小(填“偏大”、“偏小”、“无影响”).
(3)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和反应热数值会偏小(填“偏大”、“偏小”或“无影响”);
(4)取50mLNaOH溶液和30mL硫酸进行实验,实验数据如下表.
①请填写下表
②近似认为0.50 mol/L NaOH溶液和0.50 mol/L H2SO4溶液的密度都是1 g/cm3,中和后生成溶液的比热容c=4.18J/(g•℃).则中和热△H=-53.5kJ/mol(取小数点后一位).

(1)从实验装置上看,图中尚缺少的一种玻璃仪器是环形玻璃搅拌棒.
(2)大烧杯上如不盖硬纸板,求得的中和反应热数值偏小(填“偏大”、“偏小”、“无影响”).
(3)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和反应热数值会偏小(填“偏大”、“偏小”或“无影响”);
(4)取50mLNaOH溶液和30mL硫酸进行实验,实验数据如下表.
实验次数[来源:Zxxk.Com] 温度 | 起始温度t1/℃ | 终止温度t2/℃ | 平均温度差(t2-t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
②近似认为0.50 mol/L NaOH溶液和0.50 mol/L H2SO4溶液的密度都是1 g/cm3,中和后生成溶液的比热容c=4.18J/(g•℃).则中和热△H=-53.5kJ/mol(取小数点后一位).
13.下列状态时,能够导电的电解质是( )
0 172233 172241 172247 172251 172257 172259 172263 172269 172271 172277 172283 172287 172289 172293 172299 172301 172307 172311 172313 172317 172319 172323 172325 172327 172328 172329 172331 172332 172333 172335 172337 172341 172343 172347 172349 172353 172359 172361 172367 172371 172373 172377 172383 172389 172391 172397 172401 172403 172409 172413 172419 172427 203614
| A. | 石墨 | B. | 熔融态的氯化钠 | C. | 硫酸铜溶液 | D. | 干冰 |

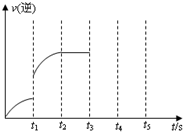 一定温度下在体积为5L的密闭容器中发生可逆反应.
一定温度下在体积为5L的密闭容器中发生可逆反应.