19.CO2和CH4是两种重要的温室气体,通过CH4和CO2反应可以制造更高价值化学品,例如:
CO2(g)+CH4(g)?2CO(g)+2H2(g)△H=+183.4kJ•mol-1
(1)已知该反应在一定条件下能自发进行,则下列说法正确的是②(填代号)
①该反应△S>0,反应条件为低温;
②该反应△S>0,反应条件为高温;
③该反应△S<0,反应条件为低温;
④该反应△S<0,反应条件为高温
(2)如图1表示该反应在某一时间段中反应速率与反应过程的关系图(t2、t4、t5时刻改变的条件都只有一个,且各不相同).各阶段平衡时对应的平衡常数如表所示:
请判断K1、K2、K3、K4之间的关系为K1=K2=K3>K4.(用“>”、“<”或“=”连接).
(3)若该反应在某恒温恒容容器中进行,加入一定量的CO2,在图2中画出随起始CH4物质的量增加,平衡时H2百分含量的变化曲线.

(4)某温度下,向1L恒容密闭容器中通入1mol CO2、1mol CH4,发生如下反应:CO2(g)+CH4(g)?2CO(g)+2H2(g).3分钟后达平衡,测得CH4体积分数为25%,CO2转化率为α.
①3分钟内用氢气表示的化学反应速率为V(H2)=0.22mol•L-1•min-1,CO2转化率为α=0.33(结果均保留两位有效数字).
②其他条件不变,改为加入3mol CO2、3mol CH4,平衡时CO2的转化率会小于α.(填“大于”、“小于”、“等于”或“无法判断”)
③其他条件不变,如果起始时各物质的浓度如表
则从投料开始至达到平衡状态的反应过程中会放出(填“吸收”或“放出”)热量.
CO2(g)+CH4(g)?2CO(g)+2H2(g)△H=+183.4kJ•mol-1
(1)已知该反应在一定条件下能自发进行,则下列说法正确的是②(填代号)
①该反应△S>0,反应条件为低温;
②该反应△S>0,反应条件为高温;
③该反应△S<0,反应条件为低温;
④该反应△S<0,反应条件为高温
(2)如图1表示该反应在某一时间段中反应速率与反应过程的关系图(t2、t4、t5时刻改变的条件都只有一个,且各不相同).各阶段平衡时对应的平衡常数如表所示:
| t1~t2 | t3~t4 | t4~t5 | t6~t7 |
| K1 | K2 | K3 | K4 |
(3)若该反应在某恒温恒容容器中进行,加入一定量的CO2,在图2中画出随起始CH4物质的量增加,平衡时H2百分含量的变化曲线.

(4)某温度下,向1L恒容密闭容器中通入1mol CO2、1mol CH4,发生如下反应:CO2(g)+CH4(g)?2CO(g)+2H2(g).3分钟后达平衡,测得CH4体积分数为25%,CO2转化率为α.
①3分钟内用氢气表示的化学反应速率为V(H2)=0.22mol•L-1•min-1,CO2转化率为α=0.33(结果均保留两位有效数字).
②其他条件不变,改为加入3mol CO2、3mol CH4,平衡时CO2的转化率会小于α.(填“大于”、“小于”、“等于”或“无法判断”)
③其他条件不变,如果起始时各物质的浓度如表
| 物质 | CO2 | CH4 | CO | H2 |
| 浓度(mol•L-1) | 1 | 1 | 1 | 1 |
16.实验室以含有少量铁的粗铜粉和硫酸与硝酸的混合溶液为原料制备CuSO4•5H2O(胆矾)晶体.设计的工艺流程图如图1:
请回答下列问题:
(1)根据反应原理,操作①所需的混酸溶液中硝酸和硫酸的理论配比(物质的量之比)为2:3.操作②中需要把NO与O2气体混合通入水中,混入该气体的目的是2NO+O2=2NO2、4NO2+O2+2H2O=4HNO3(用化学方程式表示).
(2)溶液I中存在一定浓度的Fe3+、Cu2+,在该浓度时生成氢氧化物沉淀的pH如右表.操作③中某学生设计物质X为H2O,若加水调整溶液pH,则Fe(OH)3开始沉淀的pH=1.9(填“<”、“>”或“=”);而实际操作中一般不用此法调节溶液pH,其主要原因是不利于蒸发浓缩.
(3)操作④中物质Y为稀硫酸.查阅资料知CuSO4•5H2O的溶解度曲线如图2所示,则操作⑤应采取的措施是蒸发浓缩、冷却结晶、过滤、洗涤、干燥等.
(4)为测定胆矾中结晶水的数目,称取25.0g胆矾品体在坩埚中加热,固体质量随温度升高而变化的曲线如图3.当固体质量为8.0g时,观察到固体完全呈黑色.请列式计算开始称取的胆矾中结晶水的数目.

请回答下列问题:
(1)根据反应原理,操作①所需的混酸溶液中硝酸和硫酸的理论配比(物质的量之比)为2:3.操作②中需要把NO与O2气体混合通入水中,混入该气体的目的是2NO+O2=2NO2、4NO2+O2+2H2O=4HNO3(用化学方程式表示).
(2)溶液I中存在一定浓度的Fe3+、Cu2+,在该浓度时生成氢氧化物沉淀的pH如右表.操作③中某学生设计物质X为H2O,若加水调整溶液pH,则Fe(OH)3开始沉淀的pH=1.9(填“<”、“>”或“=”);而实际操作中一般不用此法调节溶液pH,其主要原因是不利于蒸发浓缩.
| 开始沉淀 | 沉淀完全 | |
| Fe3+ | 1.9 | 3.2 |
| Cu2+ | 4.7 | 6.7 |
(4)为测定胆矾中结晶水的数目,称取25.0g胆矾品体在坩埚中加热,固体质量随温度升高而变化的曲线如图3.当固体质量为8.0g时,观察到固体完全呈黑色.请列式计算开始称取的胆矾中结晶水的数目.

14.葡萄糖酸钙是一种可促进骨骼生长的营养物质.葡萄糖酸钙可通过以下反应制得:
CH2OH(CHOH)4CHO+Br2+H2O→C6H12O7(葡萄糖酸)+2HBr
2C6H12O7(葡萄糖酸)+CaCO3→Ca(C6H11O7)2(葡萄糖酸钙)+H2O+CO2↑
相关物质的溶解性见下表:
实验流程如下:
葡萄糖溶液滴加3%溴水/55℃:①过量CaCO3/70℃②趁热过滤 ③乙醇 ④悬浊液
抽滤⑤洗涤⑥干燥⑦Ca(C6H11O7)2
葡萄糖溶液$→_{①}^{滴加3%溴水/55℃}$ $\underset{\stackrel{过量CaC{O}_{3}/70℃}{→}}{②}$ $→_{③}^{趁热过滤}$ $→_{④}^{乙醇}$ 悬浊液$→_{⑤}^{抽滤}$ $→_{⑥}^{洗涤}$$→_{⑦}^{干燥}$Ca(C6H11O7)2
请回答下列问题:
(1)第 ①步中溴水氧化葡萄糖时,下列装置最合适的是B(填序号).
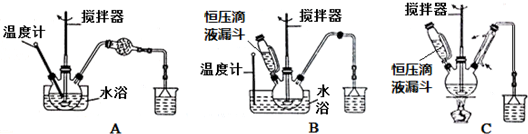
(2)第 ②步充分反应后CaCO3固体需有剩余,其目的是提高葡萄糖酸的转化率,且过量的碳酸钙易除去.
(3)本实验中不宜用CaCl2替代CaCO3,理由是氯化钙难以与葡萄糖酸直接反应制得葡萄糖酸钙.
(4)第 ③步需趁热过滤,其原因是葡萄糖酸钙冷却后会结晶析出,如不趁热过滤或损失产品.
(5)葡萄糖溶液与新制Cu(OH)2悬浊液反应的化学方程式为CH2OH(CHOH)4CHO+2Cu(OH)2+NaOH$\stackrel{△}{→}$CH2OH(CHOH)4COONa+Cu2O↓+3H2O.
CH2OH(CHOH)4CHO+Br2+H2O→C6H12O7(葡萄糖酸)+2HBr
2C6H12O7(葡萄糖酸)+CaCO3→Ca(C6H11O7)2(葡萄糖酸钙)+H2O+CO2↑
相关物质的溶解性见下表:
| 物质名称 | 葡萄糖酸钙 | 葡萄糖酸 | 溴化钙 | 氯化钙 |
| 水中的溶解性 | 可溶于冷水易溶于热水 | 可溶 | 易溶 | 易溶 |
| 乙醇中的溶解性 | 微溶 | 微溶 | 可溶 | 可溶 |
葡萄糖溶液滴加3%溴水/55℃:①过量CaCO3/70℃②趁热过滤 ③乙醇 ④悬浊液
抽滤⑤洗涤⑥干燥⑦Ca(C6H11O7)2
葡萄糖溶液$→_{①}^{滴加3%溴水/55℃}$ $\underset{\stackrel{过量CaC{O}_{3}/70℃}{→}}{②}$ $→_{③}^{趁热过滤}$ $→_{④}^{乙醇}$ 悬浊液$→_{⑤}^{抽滤}$ $→_{⑥}^{洗涤}$$→_{⑦}^{干燥}$Ca(C6H11O7)2
请回答下列问题:
(1)第 ①步中溴水氧化葡萄糖时,下列装置最合适的是B(填序号).

(2)第 ②步充分反应后CaCO3固体需有剩余,其目的是提高葡萄糖酸的转化率,且过量的碳酸钙易除去.
(3)本实验中不宜用CaCl2替代CaCO3,理由是氯化钙难以与葡萄糖酸直接反应制得葡萄糖酸钙.
(4)第 ③步需趁热过滤,其原因是葡萄糖酸钙冷却后会结晶析出,如不趁热过滤或损失产品.
(5)葡萄糖溶液与新制Cu(OH)2悬浊液反应的化学方程式为CH2OH(CHOH)4CHO+2Cu(OH)2+NaOH$\stackrel{△}{→}$CH2OH(CHOH)4COONa+Cu2O↓+3H2O.
13. 实验室制备1,2-二溴乙烷的反应原理如下:
实验室制备1,2-二溴乙烷的反应原理如下:
CH3CH2OH $→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O
CH2=CH2+Br2→BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示,有关数据列表如下:
回答下列问题:
(1)在此制备实验中,要尽可能迅速地把反应温度提高170℃左右,其最主要目的是d.
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)判断该制备反应已经结束的最简单方法是溴的颜色完全褪去.
(3)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在层下(填“上”、“下”).
(4)若产物中有少量副产物乙醚,可用的方法除去蒸馏.
(5)反应过程中应用冷水冷却装置D,其主要目的是;但又不能过度冷却(如用冰水),其原因是避免溴大量挥发;产品1,2-二溴乙烷的熔点(凝固点)低,过度冷却会凝固而堵塞导管.
0 172223 172231 172237 172241 172247 172249 172253 172259 172261 172267 172273 172277 172279 172283 172289 172291 172297 172301 172303 172307 172309 172313 172315 172317 172318 172319 172321 172322 172323 172325 172327 172331 172333 172337 172339 172343 172349 172351 172357 172361 172363 172367 172373 172379 172381 172387 172391 172393 172399 172403 172409 172417 203614
 实验室制备1,2-二溴乙烷的反应原理如下:
实验室制备1,2-二溴乙烷的反应原理如下:CH3CH2OH $→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O
CH2=CH2+Br2→BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示,有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态、溶解性 | 无色液体、易溶于水 | 无色液体 | 无色液体、难溶于水 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -l30 | 9 | -1l6 |
(1)在此制备实验中,要尽可能迅速地把反应温度提高170℃左右,其最主要目的是d.
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)判断该制备反应已经结束的最简单方法是溴的颜色完全褪去.
(3)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在层下(填“上”、“下”).
(4)若产物中有少量副产物乙醚,可用的方法除去蒸馏.
(5)反应过程中应用冷水冷却装置D,其主要目的是;但又不能过度冷却(如用冰水),其原因是避免溴大量挥发;产品1,2-二溴乙烷的熔点(凝固点)低,过度冷却会凝固而堵塞导管.


 ,其电子的自旋方向共有2种.比较两种同主族非金属元素形成的单质的氧化性(用化学方程式表示)2H2S+O2=2S↓+2H2O
,其电子的自旋方向共有2种.比较两种同主族非金属元素形成的单质的氧化性(用化学方程式表示)2H2S+O2=2S↓+2H2O
