15. 有可逆反应mA(s)+nB(g)═pC(g)+qD(g),反应过程中,当其它条件不变时,C的质量分数与温度(T)和压强(P)的关系如图所示,根据图中曲线分析,判断下列叙述中,正确的是( )
有可逆反应mA(s)+nB(g)═pC(g)+qD(g),反应过程中,当其它条件不变时,C的质量分数与温度(T)和压强(P)的关系如图所示,根据图中曲线分析,判断下列叙述中,正确的是( )
 有可逆反应mA(s)+nB(g)═pC(g)+qD(g),反应过程中,当其它条件不变时,C的质量分数与温度(T)和压强(P)的关系如图所示,根据图中曲线分析,判断下列叙述中,正确的是( )
有可逆反应mA(s)+nB(g)═pC(g)+qD(g),反应过程中,当其它条件不变时,C的质量分数与温度(T)和压强(P)的关系如图所示,根据图中曲线分析,判断下列叙述中,正确的是( )| A. | 到达平衡后,若使用催化剂,C的质量分数增大 | |
| B. | 平衡后,若升高温度,平衡则向逆反应方向移动 | |
| C. | 平衡后增大A的量,有利于提高A的转化率 | |
| D. | 化学方程式中一定是m+n<p+q |
13.具备基本的实验技能是进行科学探究活动的基础.下列有关实验操作正确的是( )
| A. |  点燃洒精灯 | B. |  称量10.05g固体 | C. | 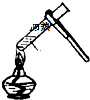 液体加热 | D. |  倾倒液体 |
8.室温时,M(OH)2(S)?M2+(aq)+2OH-(aq) Ksp=a,C(M2+)=b m ol/L时,溶液的pH等于(已知lg2=0.3)( )
| A. | $\frac{1}{2}$lg($\frac{b}{a}$) | B. | 14.3+lgb | C. | 14+$\frac{1}{2}$lg($\frac{a}{b}$) | D. | 14+$\frac{1}{2}$lg($\frac{b}{a}$) |
7.有四种短周期元素,它们的结构、性质等信息如下表所述:
请根据表中信息填写:
(1)A原子的核外电子排布式1s22s22p63s1.
(2)B元素在周期表中的位置第3周期第ⅢA族;离子半径:B小于A(填“大于”或“小于”).
(3)C原子的电子排布图是 ,其原子核外有3个未成对电子,能量最高的电子为p轨道上的电子,其轨道呈哑铃形.
,其原子核外有3个未成对电子,能量最高的电子为p轨道上的电子,其轨道呈哑铃形.
(4)D-的结构示意图是 .
.
(5)B的最高价氧化物对应的水化物与A的最高价氧化物对应的水化物反应的化学方程式为Al(OH)3+NaOH═NaAlO2+2H2O,与D的氢化物的水化物反应的化学方程式为Al(OH)3+3HCl═AlCl3+3H2O.
0 172199 172207 172213 172217 172223 172225 172229 172235 172237 172243 172249 172253 172255 172259 172265 172267 172273 172277 172279 172283 172285 172289 172291 172293 172294 172295 172297 172298 172299 172301 172303 172307 172309 172313 172315 172319 172325 172327 172333 172337 172339 172343 172349 172355 172357 172363 172367 172369 172375 172379 172385 172393 203614
| 元素 | 结构、性质等信息 |
| A | 是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂 |
| B | B与A同周期,其最高价氧化物的水化物呈两性 |
| C | 元素的气态氢化物极易溶于水,可用作制冷剂 |
| D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂 |
(1)A原子的核外电子排布式1s22s22p63s1.
(2)B元素在周期表中的位置第3周期第ⅢA族;离子半径:B小于A(填“大于”或“小于”).
(3)C原子的电子排布图是
 ,其原子核外有3个未成对电子,能量最高的电子为p轨道上的电子,其轨道呈哑铃形.
,其原子核外有3个未成对电子,能量最高的电子为p轨道上的电子,其轨道呈哑铃形.(4)D-的结构示意图是
 .
.(5)B的最高价氧化物对应的水化物与A的最高价氧化物对应的水化物反应的化学方程式为Al(OH)3+NaOH═NaAlO2+2H2O,与D的氢化物的水化物反应的化学方程式为Al(OH)3+3HCl═AlCl3+3H2O.
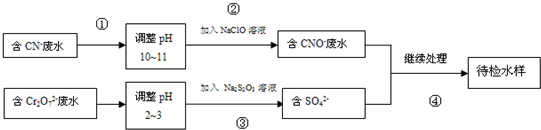
 如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:
如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:

 ;
; +CH3CH(OH)CH2CH2OH$→_{△}^{浓硫酸}$
+CH3CH(OH)CH2CH2OH$→_{△}^{浓硫酸}$ +2H2O;
+2H2O; .
.
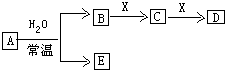 由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如图转化关系(部分生成物和反应条件略去).
由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如图转化关系(部分生成物和反应条件略去). ;
;