17.某小组用如图装置进行实验,下列说法正确的是( )
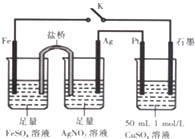

| A. | 盐桥中的电解质可以用KC1 | |
| B. | 导线中流过0.2mol电子时,加入4.9gCu(OH)2,CuSO4溶液可恢复原组成 | |
| C. | 闭合K,石墨电极上只生成铜 | |
| D. | 闭合K,外电路电流方向为Fe电极→石墨电极 |
16.常温下有0.1mol/L的以下几种溶液,①H2SO4溶液,②NaHSO4溶液,③CH3COOH溶液,④HCl溶液,⑤HCN溶液,⑥NH3•H2O,其中如下几种溶液的电离度(即已经电离的占原来总的百分数)如下表(已知H2SO4的第一步电离是完全的),回答下面问题:
(1)常温下,pH相同的表格中几种溶液,其物质的量浓度由大到小的顺序是③>②>④>①(填序号,下同)
(2)常温下,将足量的锌粉投人等体积pH=1的表格中几种溶液中,产生H2的体积(同温同压下)由大到小的顺序是③>②>①>④
(3)在25℃时,若用已知浓度的NaOH滴定未知浓度的CH3 COOH,若终点时溶液pH=a,则由水电离的.c(H+)为10-amol/L.
(4)25℃时,将amol NH4NO3溶于水,溶液显酸性,向该溶液滴加bL氨水后溶液呈中性,则滴加氨水的过程中的水的电离平衡将逆向(填“正向”“不”或“逆向”)移动,所滴加氨水的浓度为$\frac{a}{200b}$mol•L-1.(NH3•H2O的电离平衡常数取Kb=2X10-5 mol•L-1)
| ①H2SO4溶液HSO4- | ②NaHSO4溶液HSO4- | ③CH3COOH | ④HCl溶液 |
| 10% | 29% | 1.33% | 100% |
(2)常温下,将足量的锌粉投人等体积pH=1的表格中几种溶液中,产生H2的体积(同温同压下)由大到小的顺序是③>②>①>④
(3)在25℃时,若用已知浓度的NaOH滴定未知浓度的CH3 COOH,若终点时溶液pH=a,则由水电离的.c(H+)为10-amol/L.
(4)25℃时,将amol NH4NO3溶于水,溶液显酸性,向该溶液滴加bL氨水后溶液呈中性,则滴加氨水的过程中的水的电离平衡将逆向(填“正向”“不”或“逆向”)移动,所滴加氨水的浓度为$\frac{a}{200b}$mol•L-1.(NH3•H2O的电离平衡常数取Kb=2X10-5 mol•L-1)
14.同温同压下,等质量的SO2和CO2相比较,下列叙述正确的是( )
| A. | 体积比 1:1 | B. | 体积比 11:16 | ||
| C. | 物质的量比 16:11 | D. | 密度比 11:16 |
13.下列叙述正确的是( )
| A. | 1.00 mol NaCl 中含有 6.02×1023个分子 | |
| B. | 1.00 mol NaCl 中,所有Na+的电子总数为 10×6.02×1023 | |
| C. | 欲配制 1.00 L 1.00 mol/L 的NaCl溶液,可将 58.5gNaCl溶于 1.00L 水中 | |
| D. | 电解 58.5g 熔融的 NaCl,能产生22.4L氯气(标准状况)、23.0g 金属钠 |
10.下列说法正确的是( )
| A. | 由H原子形成1 mol H-H键要吸收热量 | |
| B. | 所有燃烧反应都是放热反应 | |
| C. | 在稀溶液中,1 mol酸与1 mol碱发生中和反应生成水时所释放的热量称为中和热 | |
| D. | 在一定条件下,1mol H2 与足量的Cl2、Br2、I2 分别反应,放出热量关系是I2>Br2>Cl2 |
8.下列各选项中,前者属于电解质,后者属于非电解质的是( )
0 172161 172169 172175 172179 172185 172187 172191 172197 172199 172205 172211 172215 172217 172221 172227 172229 172235 172239 172241 172245 172247 172251 172253 172255 172256 172257 172259 172260 172261 172263 172265 172269 172271 172275 172277 172281 172287 172289 172295 172299 172301 172305 172311 172317 172319 172325 172329 172331 172337 172341 172347 172355 203614
| A. | NaOH、氯气 | B. | 盐酸、蔗糖 | C. | 熔融NaCl、酒精 | D. | 二氧化碳、BaSO4 |
 有如图实验装置,其中a、b、c为弹簧夹.
有如图实验装置,其中a、b、c为弹簧夹.