18.某地酸雨经检验除含H+外[C(OH)-以及其他微量的离子浓度忽略]还有Na+,Cl-,NH4+,SO42-其浓度见表:
(1)试计算混合液中H+的浓度3.5×10-3mol•L-1.
(2)取1mL该酸雨,若完全反应消耗NaOH的物质的量为3.5×10-6mol.
(3)若只用一份该酸雨样品检验其中Cl-和SO42-应先加Ba(OH)2(填化学式)待沉淀完全后再加AgNO3(填化学式).
(4)在问题(3)中判断已沉淀完全可加第二份沉淀剂的具体操作方法为取加入氢氧化钡以后的溶液少量,向其中加入少量的盐酸,看是否产生无色气体,若没有气体产生,证明硫酸根离子沉淀完全.
| 离子种类 | Na+ | Cl- | NH4+ | SO42- |
| 离子浓度 | 2.3×10-5mol/L | 3.5×10-5mol/L | 7×10-6mol/L | 2.4×10-6mol/L |
(2)取1mL该酸雨,若完全反应消耗NaOH的物质的量为3.5×10-6mol.
(3)若只用一份该酸雨样品检验其中Cl-和SO42-应先加Ba(OH)2(填化学式)待沉淀完全后再加AgNO3(填化学式).
(4)在问题(3)中判断已沉淀完全可加第二份沉淀剂的具体操作方法为取加入氢氧化钡以后的溶液少量,向其中加入少量的盐酸,看是否产生无色气体,若没有气体产生,证明硫酸根离子沉淀完全.
15.下列物质间的转化不能通过一步转化实现的是( )
| A. | Na2CO3→Na0H | B. | Fe→Cu | C. | Cu→Cu(OH)2 | D. | CaCl2→CaCO3 |
14.物质M在水中发生如下电离:M=X2++2Y-,则下列判断正确的是( )
| A. | M一定不是酸 | B. | X2+一定是金属离子 | ||
| C. | Y-是OH- | D. | M是一定属于盐 |
10.25℃、101kPa下,二氧化碳和过氧化钠反应后,若固体质量增加了14g,反应中有关物质的物理量正确的是( )
0 171823 171831 171837 171841 171847 171849 171853 171859 171861 171867 171873 171877 171879 171883 171889 171891 171897 171901 171903 171907 171909 171913 171915 171917 171918 171919 171921 171922 171923 171925 171927 171931 171933 171937 171939 171943 171949 171951 171957 171961 171963 171967 171973 171979 171981 171987 171991 171993 171999 172003 172009 172017 203614
| O2 | Na2CO3 | CO2 | 转移电子数 | |
| A | 1mol | 0.5NA | ||
| B | 0.5mol | 11.2L | ||
| C | 0.25mol | 53g | ||
| D | 8g | NA |
| A. | A | B. | B | C. | C | D. | D |
 肉桂酸(
肉桂酸(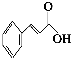 )在化妆行业及香料行业中属于明星物质,而且其需求量愈来愈大,如图是该物质的合成及其应用.根据图示回答下列问题:
)在化妆行业及香料行业中属于明星物质,而且其需求量愈来愈大,如图是该物质的合成及其应用.根据图示回答下列问题: ,其分子中所有的碳原子是否可能处于同一个平面?可能(填“可能”或“不可能”).
,其分子中所有的碳原子是否可能处于同一个平面?可能(填“可能”或“不可能”).  +
+ $→_{△}^{浓H_{2}SO_{4}}$
$→_{△}^{浓H_{2}SO_{4}}$ +H2O.
+H2O.