题目内容
11.现欲配制500mL 1.0mol/L NaOH溶液,需称取NaOH固体多少?若用4.0mol/L NaOH溶液稀释得到,则量取4.0mol/L NaOH溶液体积多少毫升?分析 依据m=CVM计算氢氧化钠的质量;依据溶液稀释前后溶质的物质的量不变计算需要浓溶液的体积,据此解答.
解答 解:配制500mL 1.0mol/L NaOH溶液,需称取NaOH固体=1.0mol/L×0.5L×40g/mol=20.0g;
若用4.0mol/L NaOH溶液稀释得到,则量取4.0mol/L NaOH溶液体积为V,则依据溶液稀释前后溶质的物质的量不变得:500mL×1.0mol/L=4.0mol/L×V
解得V=125.0mL;
答:欲配制500mL 1.0mol/L NaOH溶液,需称取NaOH固体20.0g;
若用4.0mol/L NaOH溶液稀释得到,则量取4.0mol/L NaOH溶液体积125.0mL.
点评 本题考查了有关物质的量浓度计算,熟悉相关公式及溶液稀释规律是解题关键,题目难度不大.

练习册系列答案
相关题目
8.CH2=CH-CH=C(CH3)-CH=CH2与等物质的量的Br2加成时可能得到的异构体有( )
| A. | 5种 | B. | 2种 | C. | 3种 | D. | 4种 |
9.在一定的条件下,只用一种试剂就能区别蒸馏水、硫化钠溶液和氢氧化钠溶液,这种试剂是( )
| A. | 碳酸钠溶液 | B. | 氯化铁溶液 | C. | 硝酸钡溶液 | D. | 硝酸钙溶液 |
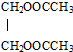 (过程中无机产物已忽略)
(过程中无机产物已忽略) .
. 现有14.4g CO和CO2的混合气体,在标准状况下其体积为8.96L.回答下列问题:
现有14.4g CO和CO2的混合气体,在标准状况下其体积为8.96L.回答下列问题: 肉桂酸(
肉桂酸(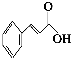 )在化妆行业及香料行业中属于明星物质,而且其需求量愈来愈大,如图是该物质的合成及其应用.根据图示回答下列问题:
)在化妆行业及香料行业中属于明星物质,而且其需求量愈来愈大,如图是该物质的合成及其应用.根据图示回答下列问题: ,其分子中所有的碳原子是否可能处于同一个平面?可能(填“可能”或“不可能”).
,其分子中所有的碳原子是否可能处于同一个平面?可能(填“可能”或“不可能”).  +
+ $→_{△}^{浓H_{2}SO_{4}}$
$→_{△}^{浓H_{2}SO_{4}}$ +H2O.
+H2O.