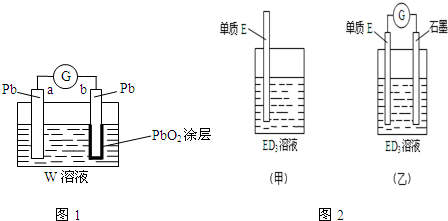
9.下列化合物不能通过化合反应获得的是( )
| A. | Fe(OH)3 | B. | Al(OH)3 | C. | HCl | D. | NaHCO3 |
8.重庆市每天都会发布“空气质量日报”.下列中不列入首要污染物的是( )
| A. | 二氧化硫 | B. | 二氧化碳 | C. | 二氧化氮 | D. | 可吸入颗粒 |
5.既可以用来鉴别甲烷和乙烯,又可以用来除去乙烷中混有的乙烯,得到纯净乙烷的方法( )
| A. | 与足量酸性高锰酸钾反应 | B. | 依次通入通入足量溴水和浓硫酸中 | ||
| C. | 在一定条件下通入H2 | D. | 分别进行燃烧 |
4.如图为短周期的一部分,Y原子最外层电子数是其电子层数的2倍,下列说法正确的是(
| R | ||
| X | Y | Z |
| A. | Y的氢化物比Z的氢化物稳定 | |
| B. | 原子半径大小顺序是X>Y>R | |
| C. | Y、R形成的化台物YR3能使酸性KMnO4溶液褪色 | |
| D. | 四种元素中最高价氧化物的水化物的酸性最强的是Y |
3.在一定条件下,对于密闭容器中进行的反应:2SO2(g)+O2(g)?2SO3(g),下列说法能充分说明该反应已达到化学平衡状态的是( )
| A. | 正、逆反应速率都等于零 | B. | SO2、O2、SO3的浓度相等 | ||
| C. | SO2、O2、SO3在容器中共存 | D. | SO2、O2、SO3的浓度均不再变化 |
2.原子序数小于18的元素X,其原子最外层中未成对电子数最多,含这种元素的阴离子可能是( )
| A. | XO3- | B. | XO32- | C. | XO42- | D. | XO43- |
20.氯化亚铜(CuCl)常用作有机合成工业中的催化剂,在空气中迅速被氧化成绿色;见光则分解,变成褐色.如图是工业上用制作印刷电路的废液(含Fe3+、Cu2+、Fe2+、Cl-)生产CuCl的流程:

根据以上信息回答下列问题:
(1)写出生产过程中XFe YHCl(填化学式).
(2)写出产生CuCl的化学方程式CuCl2+CuSO4+SO2+2H2O=2CuCl↓+2H2SO4.
(3)在CuCl的生成过程中理论上不需要补充SO2气体,结合化学方程式和必要的文字说明理由Cu+2 H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ CuSO4+SO2↑+2H2O反应中生成的CuSO4和 SO2为1:1,所以理论上不需要补充SO2气体.
(4)在CuCl的生成过程中除环境问题、安全问题外,你认为还应该注意的关键问题是生产中应防止CuCl的氧化和见光分解,减少产品CuCl的损失.
(5)实验探究pH对CuCl产率的影响如下表所示:
析出CuCl晶体最佳pH为2,当pH较大时CuCl产率变低原因是pH较大时,Cu2+水解程度增大,反应生成CuCl减少.
(6)氯化亚铜的定量分析:
①称取样品0.25g和10mL过量的FeCl3溶液250mL于锥形瓶中,充分溶解.
②用0.10mol•L-1硫酸铈[Ce(SO4)2]标准溶液滴定.已知:CuCl+FeCl3=CuCl2+FeCl2、Fe2++Ce4+=Fe3++Ce3+.三次平行实验结果如下(平行实验结果相差不能超过1%):
则样品中CuCl的纯度为95.5%(结果保留三位有效数字).
0 168158 168166 168172 168176 168182 168184 168188 168194 168196 168202 168208 168212 168214 168218 168224 168226 168232 168236 168238 168242 168244 168248 168250 168252 168253 168254 168256 168257 168258 168260 168262 168266 168268 168272 168274 168278 168284 168286 168292 168296 168298 168302 168308 168314 168316 168322 168326 168328 168334 168338 168344 168352 203614

根据以上信息回答下列问题:
(1)写出生产过程中XFe YHCl(填化学式).
(2)写出产生CuCl的化学方程式CuCl2+CuSO4+SO2+2H2O=2CuCl↓+2H2SO4.
(3)在CuCl的生成过程中理论上不需要补充SO2气体,结合化学方程式和必要的文字说明理由Cu+2 H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ CuSO4+SO2↑+2H2O反应中生成的CuSO4和 SO2为1:1,所以理论上不需要补充SO2气体.
(4)在CuCl的生成过程中除环境问题、安全问题外,你认为还应该注意的关键问题是生产中应防止CuCl的氧化和见光分解,减少产品CuCl的损失.
(5)实验探究pH对CuCl产率的影响如下表所示:
| pH | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| CuCl产率 | 70 | 90 | 82 | 78 | 75 | 72 | 70 |
(6)氯化亚铜的定量分析:
①称取样品0.25g和10mL过量的FeCl3溶液250mL于锥形瓶中,充分溶解.
②用0.10mol•L-1硫酸铈[Ce(SO4)2]标准溶液滴定.已知:CuCl+FeCl3=CuCl2+FeCl2、Fe2++Ce4+=Fe3++Ce3+.三次平行实验结果如下(平行实验结果相差不能超过1%):
| 平行实验次数 | 1 | 2 | 3 |
| 0.25g样品消耗硫酸铈标准溶液的体积(mL) | 24.35 | 24.05 | 23.95 |
 ;
; 的系统命名为2,5-二甲基-3-乙基庚烷.
的系统命名为2,5-二甲基-3-乙基庚烷. .
.