15.甲醇合成反应为:CO(g)+2H2(g)?CH3OH(g)
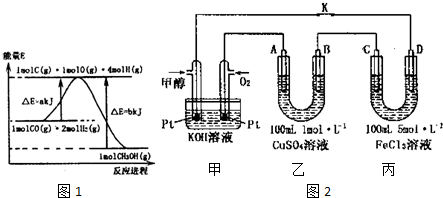
(1)合成甲醇的反应过程中物质能量变化如图1所示.写出合成甲醇的热化学方程式CO(g)+2H2(g)?CH3OH(g)△H=-(b-a)kJ/mol.
(2)实验室在lL密闭容器中进行模拟合成实验.将1molCO和2molH2通入容器中,分别恒温在300℃和500℃反应,每隔一定时间测得容器中甲醇的浓度如下:(表中数据单位:mol•L-l)
①300℃时反应开始10分钟内,H2的平均反应速率为0.08mol/(L•min);
②500℃时平衡常数K的数值为25;
③300℃时,将容器的容积压缩到原来的$\frac{1}{2}$,在其他条件不变的情况下,对平衡体系产生的影响是cd(选填编号).
a.c(H2)减小
b.正反应速率加快,逆反应速率减慢
c.CH3OH的物质的量增加
d.重新平衡时$\frac{c({H}_{2})}{c(C{H}_{3}OH)}$减小
(3)如图2是甲醇燃料电池工作的示意图,其中A、B、D均为石墨电极,C为铜电极.工作一段时间后,断开K,此时A、B两极上产生的气体体积相同.
①甲中负极的电极反应式为CH3OH-6e-+8OH-=CO32-+6H2O;
②乙中A极析出的气体在标准状况下的体积为2.24l;
③反应结束后,要使丙装置中金属阳离子恰好完全沉淀,需要300mL5.0mol•L-lNaOH 溶液.

(1)合成甲醇的反应过程中物质能量变化如图1所示.写出合成甲醇的热化学方程式CO(g)+2H2(g)?CH3OH(g)△H=-(b-a)kJ/mol.
(2)实验室在lL密闭容器中进行模拟合成实验.将1molCO和2molH2通入容器中,分别恒温在300℃和500℃反应,每隔一定时间测得容器中甲醇的浓度如下:(表中数据单位:mol•L-l)
| 温度\时间 | 10min | 20min | 30min | 40min | 50min | 60min |
| 300℃ | 0.40 | 0.60 | 0.75 | 0.84 | 0.90 | 0.90 |
| 500℃ | 0.60 | 0.75 | 0.78 | 0.80 | 0.80 | 0.80 |
②500℃时平衡常数K的数值为25;
③300℃时,将容器的容积压缩到原来的$\frac{1}{2}$,在其他条件不变的情况下,对平衡体系产生的影响是cd(选填编号).
a.c(H2)减小
b.正反应速率加快,逆反应速率减慢
c.CH3OH的物质的量增加
d.重新平衡时$\frac{c({H}_{2})}{c(C{H}_{3}OH)}$减小
(3)如图2是甲醇燃料电池工作的示意图,其中A、B、D均为石墨电极,C为铜电极.工作一段时间后,断开K,此时A、B两极上产生的气体体积相同.
①甲中负极的电极反应式为CH3OH-6e-+8OH-=CO32-+6H2O;
②乙中A极析出的气体在标准状况下的体积为2.24l;
③反应结束后,要使丙装置中金属阳离子恰好完全沉淀,需要300mL5.0mol•L-lNaOH 溶液.
13.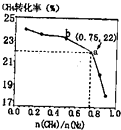 CH4、和N2在一定条件下能直接生成氨:3CH4(g)+2N2(g)$?_{催化剂}^{700℃}$3C(s)+4NH3(g)△H>0,700℃时,$\frac{n(C{H}_{4})}{n({N}_{2})}$与CH4的平衡转化率的关系如图所示.下列判断正确的是( )
CH4、和N2在一定条件下能直接生成氨:3CH4(g)+2N2(g)$?_{催化剂}^{700℃}$3C(s)+4NH3(g)△H>0,700℃时,$\frac{n(C{H}_{4})}{n({N}_{2})}$与CH4的平衡转化率的关系如图所示.下列判断正确的是( )
 CH4、和N2在一定条件下能直接生成氨:3CH4(g)+2N2(g)$?_{催化剂}^{700℃}$3C(s)+4NH3(g)△H>0,700℃时,$\frac{n(C{H}_{4})}{n({N}_{2})}$与CH4的平衡转化率的关系如图所示.下列判断正确的是( )
CH4、和N2在一定条件下能直接生成氨:3CH4(g)+2N2(g)$?_{催化剂}^{700℃}$3C(s)+4NH3(g)△H>0,700℃时,$\frac{n(C{H}_{4})}{n({N}_{2})}$与CH4的平衡转化率的关系如图所示.下列判断正确的是( )| A. | $\frac{n(C{H}_{4})}{n({N}_{2})}$越大,CH4的转化率越高 | |
| B. | $\frac{n(C{H}_{4})}{n({N}_{2})}$与不变时,升温,NH3的体积分数会减小 | |
| C. | b点对应的平衡常数比a点的大 | |
| D. | a点对应的NH3的体积分数约为13% |
12.已知平衡:
①C2H4(g)?C2H2(g)+H2(g),
②2CH4(g)?C2H4(g)+2H2(g).当升高温度时,①和②式皆向右移动.
(1)C(s)+2H2(g)?CH4(g)△H1
(2)2C(s)+H2(g)?C2H2(g)△H2
(3)2C(s)+2H2(g)?C2H4(g)△H3
下列有关(1)、(2)和(3)中的△H1、△H2、△H3大小顺序排列正确的是( )
①C2H4(g)?C2H2(g)+H2(g),
②2CH4(g)?C2H4(g)+2H2(g).当升高温度时,①和②式皆向右移动.
(1)C(s)+2H2(g)?CH4(g)△H1
(2)2C(s)+H2(g)?C2H2(g)△H2
(3)2C(s)+2H2(g)?C2H4(g)△H3
下列有关(1)、(2)和(3)中的△H1、△H2、△H3大小顺序排列正确的是( )
| A. | △H1>△H2>△H3 | B. | △H2>△H3>2△H1 | C. | △H2>△H1>△H3 | D. | △H3>△H2>2△H1 |
11.短周期主族元素X、Y、W、Z的原子序数依次增大.其中X、Z同主族,Z的单质是一种良好的半导体材料,W3+与Y2-具有相同的核外电子数.下列叙述正确的是( )
0 166856 166864 166870 166874 166880 166882 166886 166892 166894 166900 166906 166910 166912 166916 166922 166924 166930 166934 166936 166940 166942 166946 166948 166950 166951 166952 166954 166955 166956 166958 166960 166964 166966 166970 166972 166976 166982 166984 166990 166994 166996 167000 167006 167012 167014 167020 167024 167026 167032 167036 167042 167050 203614
| A. | Y2-的离子半径大于W3+的离子半径 | |
| B. | Y、Z形成的化合物为离子化合物 | |
| C. | Z的最高价氧化物对应的水化物的酸性比X的强 | |
| D. | X的气态简单氢化物的稳定性比Y的强 |

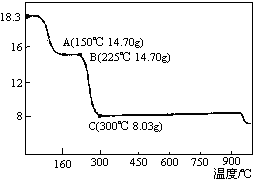 草酸钴是制备钴的氧化物的重要原料.如图为二水合草酸钴(CoC2O4•2H2O)在空气中受热的质量变化曲线,曲线中300℃及以上所得固体均为钴氧化物.
草酸钴是制备钴的氧化物的重要原料.如图为二水合草酸钴(CoC2O4•2H2O)在空气中受热的质量变化曲线,曲线中300℃及以上所得固体均为钴氧化物.

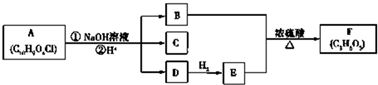
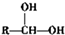 $\stackrel{自动脱水}{→}$
$\stackrel{自动脱水}{→}$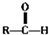 (R为羟基)
(R为羟基) .
. .
.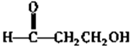 .
.