7.足量的Fe与一定量的0.5mol/L盐酸反应,为了加快反应速率,但又不影响产生氢气的总量,应加入下列物质中的( )
| A. | CuSO4溶液 | B. | 将Fe改为同质量的Na | ||
| C. | 改为用浓硫酸 | D. | NaNO3溶液 |
4.在一定条件下,反应N2+3H2?2NH3,密闭容器中进行,5min内氨的物质的量增加了0.1mol/L,则反应速率为( )
| A. | v(NH3)=0.5 mol/(L•min) | B. | v(NH3)=0.02 mol/(L•min) | ||
| C. | v(NH3)=0.1mol/(L•min) | D. | v(NH3)=0.01 mol/(L•min) |
3.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | pH=1的溶液中:Fe2+、NO3-、SO42-、Na+ | |
| B. | 由水电离的c(H+)=1×10-14mol•L-1的溶液中:Ca2+、K+、Cl-、HCO3- | |
| C. | c(H+)/c(OH-)=1012的溶液中:NH4+、Al3+、NO3-、Cl- | |
| D. | c(Fe3+)=0.1mol•L-1的溶液中:K+、ClO-、SO42-、HCO3- |
1.下列有关铁及其化合物的说法中正确的是( )
| A. | 铁的化学性质比较活泼,所以铁在自然界中全部以化化合态存在 | |
| B. | 铁在纯氧中燃烧或在氯气中燃烧所得产物中铁的化合价均为+3价 | |
| C. | 工业上可用铁质容器储存浓硝酸和浓硫酸,原因是铁在常温下与两种酸不反应 | |
| D. | 工业上用CO在高温条件下还原含Fe2O3的铁矿石炼铁 |
19.氯化亚铜(CuCl)是白色粉末,微溶于水,能与稀硫酸反应,广泛应用于化工和印染等行业.某研究性学
习小组拟热分解CuC12•2H2O制备CuCl,并进行相关探究(已知酸性条件下Cu+不稳定).

下列说法正确的是( )
0 163952 163960 163966 163970 163976 163978 163982 163988 163990 163996 164002 164006 164008 164012 164018 164020 164026 164030 164032 164036 164038 164042 164044 164046 164047 164048 164050 164051 164052 164054 164056 164060 164062 164066 164068 164072 164078 164080 164086 164090 164092 164096 164102 164108 164110 164116 164120 164122 164128 164132 164138 164146 203614
习小组拟热分解CuC12•2H2O制备CuCl,并进行相关探究(已知酸性条件下Cu+不稳定).

下列说法正确的是( )
| A. | X气体可以是N2,目的是做保护气,抑制CuCl2•2H2O加热过程可能的水解 | |
| B. | CuCl与稀硫酸反应的离子方程式为:2Cu++4H++SO42-═2Cu2++SO2↑+2H2O | |
| C. | 途径1中产生的Cl2可以回收循环利用,也可以通入饱和CaCl2溶液中除去 | |
| D. | 途径2中200℃下反应的化学方程式为:Cu2(OH)2Cl2$\frac{\underline{\;加热\;}}{\;}$2CuO+2HCl |


 .
. +Cl2$\stackrel{FeCl_{3}}{→}$
+Cl2$\stackrel{FeCl_{3}}{→}$ +HCl.
+HCl. 、
、 .
. 的合成路线.
的合成路线.
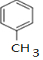 ,D中通过反应②引入的官能团名称为氯原子.
,D中通过反应②引入的官能团名称为氯原子.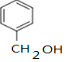 $?_{△}^{浓硫酸}$
$?_{△}^{浓硫酸}$ +H2O.
+H2O. (填结构简式).
(填结构简式).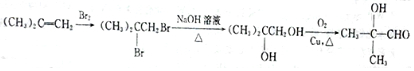 .
.
