15.下列反应既属于氧化还原反应,又是典型的放热反应的是( )
| A. | 铝粉与Fe2O3高温下反应 | B. | Ba(OH)2•8H2O与NH4Cl反应 | ||
| C. | NaOH与H2SO4的中和反应 | D. | 灼热的炭与CO2反应 |
14.下列各装置能够构成原电池的是( )
| A. |  | B. |  | ||
| C. |  | D. |  |
13.单质钛的机械强度高,抗蚀能力强,有“未来金属”之称.工业上常用硫酸分解钛铁矿(FeTiO3)的方法制取二氧化钛,再由二氧化钛制金属钛,主要反应有( )
①FeTiO3+3H2SO4═Ti(SO4)2+FeSO4+3H2O
②Ti(SO4)2+3H2O═H2TiO3↓+2H2SO4
③H2TiO3 $\stackrel{△}{→}$TiO2+H2O
④TiO2+2C+2Cl2 $\stackrel{△}{→}$ TiCl4↑+CO↑
⑤TiCl4+2Mg $\stackrel{△}{→}$ 2MgCl2+Ti
下列叙述错误的是( )
①FeTiO3+3H2SO4═Ti(SO4)2+FeSO4+3H2O
②Ti(SO4)2+3H2O═H2TiO3↓+2H2SO4
③H2TiO3 $\stackrel{△}{→}$TiO2+H2O
④TiO2+2C+2Cl2 $\stackrel{△}{→}$ TiCl4↑+CO↑
⑤TiCl4+2Mg $\stackrel{△}{→}$ 2MgCl2+Ti
下列叙述错误的是( )
| A. | 反应①属于非氧化还原反应 | |
| B. | 反应②是水解反应 | |
| C. | 反应④中二氧化钛是氧化剂 | |
| D. | 反应⑤表现了金属镁还原性比金属钛强 |
12.某同学在实验室做铜与浓硫酸反应的实验.
(1)写出反应的化学方程式2H2SO4(浓)+Cu$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O
停止加热,将试管中的混合物冷却后倒入装有冷水的烧杯中,搅拌、静置,观察到烧杯底部有黑色物质.于是他对黑色物质进行了探究.
(2)该同学假设黑色物质是CuO.检验过程如下:
【查阅文献:检验微量Cu2+的方法是:向试液中滴加K4[Fe(CN)6]溶液,若产生红褐红沉淀,证明有Cu2+】该同学的实验操作:
①将CuO放入稀硫酸中,一段时间后,滴加K4[Fe(CN)6]溶液,产生红褐色沉淀.
②将黑色物质放入稀硫酸中,一段时间后,滴加K4[Fe(CN)6]溶液,未见红褐色沉淀.
实验①的目的是做对比实验由该检验过程所得结论是黑色沉淀中不含CuO.
(3)再次假设,黑色物质是铜的硫化物.实验如下:
①现象2说明黑色物质具有还原性.
②A试管上方产生浅红棕色气体的化学方程式是2NO+O2=2NO2.
③能确认黑色沉淀中含有S元素的现象是B试管中出现白色沉淀.
(4)以上实验说明,黑色物质中存在铜的硫化物.进一步实验后证明黑色物质是CuS与Cu2S的混合物.已知1molCu2S与稀硝酸反应转移8mole-,写出试管A中Cu2S溶解的化学方程式3Cu2S+20HNO3$\frac{\underline{\;\;△\;\;}}{\;}$6Cu(NO3)2+3SO2↑+8NO↑+10H2O.
(1)写出反应的化学方程式2H2SO4(浓)+Cu$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O
停止加热,将试管中的混合物冷却后倒入装有冷水的烧杯中,搅拌、静置,观察到烧杯底部有黑色物质.于是他对黑色物质进行了探究.
(2)该同学假设黑色物质是CuO.检验过程如下:
【查阅文献:检验微量Cu2+的方法是:向试液中滴加K4[Fe(CN)6]溶液,若产生红褐红沉淀,证明有Cu2+】该同学的实验操作:
①将CuO放入稀硫酸中,一段时间后,滴加K4[Fe(CN)6]溶液,产生红褐色沉淀.
②将黑色物质放入稀硫酸中,一段时间后,滴加K4[Fe(CN)6]溶液,未见红褐色沉淀.
实验①的目的是做对比实验由该检验过程所得结论是黑色沉淀中不含CuO.
(3)再次假设,黑色物质是铜的硫化物.实验如下:
 | 现象 1A试管中黑色沉淀逐渐溶解 2A试管内上方出现浅红棕色气体 3B试管中出现白色沉淀 |
②A试管上方产生浅红棕色气体的化学方程式是2NO+O2=2NO2.
③能确认黑色沉淀中含有S元素的现象是B试管中出现白色沉淀.
(4)以上实验说明,黑色物质中存在铜的硫化物.进一步实验后证明黑色物质是CuS与Cu2S的混合物.已知1molCu2S与稀硝酸反应转移8mole-,写出试管A中Cu2S溶解的化学方程式3Cu2S+20HNO3$\frac{\underline{\;\;△\;\;}}{\;}$6Cu(NO3)2+3SO2↑+8NO↑+10H2O.
10.一种熔融碳酸盐燃料电池原理示意如图.下列有关该电池的说法正确的是( )
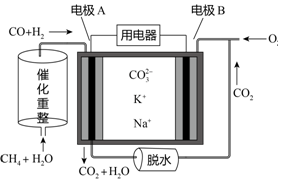

| A. | 电极A上H2和CO都发生了氧化反应 | |
| B. | 反应CH4+H2O$\frac{\underline{\;催化剂\;}}{△}$3H2+CO,每消耗1molCH4转移12mol电子 | |
| C. | 电池工作时,电能转变为化学能 | |
| D. | 电极B上发生的电极反应为:O2+2H2O+4e-═4OH- |
9.下列实验现象预测正确的是( )
| A. |  实验:振荡后静置,上层溶液颜色保持不变 | |
| B. |  实验:试管溶液中出现气泡,溶液先出现浑浊后变澄清 | |
| C. |  实验:微热稀HNO3片刻,溶液中有气泡产生,广口瓶内始终保持无色 | |
| D. | 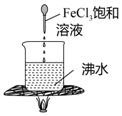 实验:加热至混合液呈红褐色,停止加热,该分散系能产生丁达尔效应 |
8.宏观物质是由微粒构成的,微粒之间存在相互作用,下列说法错误的是( )
| A. | 食盐是由Na+和Cl-通过离子键形成的离子化合物 | |
| B. | Si与C同属ⅣA族,因此SiO2和CO2两种物质中微粒间作用完全相同 | |
| C. | 含有共价键的化合物不一定是共价化合物 | |
| D. | 冰中H2O分子间存在氢键、H2O分子内存在极性共价键 |
7.某同学将铁片A和碳棒B用导线连接后放入食盐水中模拟菜刀生锈过程,则下列叙述错误的是( )
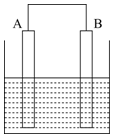

| A. | 导线中有电子流动,电流方向为A流向B | |
| B. | 溶液中的O2在电极B得电子,电极B附近碱性增强 | |
| C. | 电极A上的电极反应式为Fe-2e-=Fe2+ | |
| D. | 溶液中的Na+向电极B附近移动 |
6.用NA个表示阿伏加德罗常数的值,下列叙述正确的是( )
0 163913 163921 163927 163931 163937 163939 163943 163949 163951 163957 163963 163967 163969 163973 163979 163981 163987 163991 163993 163997 163999 164003 164005 164007 164008 164009 164011 164012 164013 164015 164017 164021 164023 164027 164029 164033 164039 164041 164047 164051 164053 164057 164063 164069 164071 164077 164081 164083 164089 164093 164099 164107 203614
| A. | 1molNa2O2固体中含有的阴离子数为2NA | |
| B. | 常温常压下,3.2gCH4中含有电子数为2NA | |
| C. | 标准状况下,11.2LCH3CH2OH中含有分子0.5NA | |
| D. | 100mL1mol•L-1的盐酸中含有HCl分子数为0.1NA |
 .
. .
. .
.