题目内容
12.某同学在实验室做铜与浓硫酸反应的实验.(1)写出反应的化学方程式2H2SO4(浓)+Cu$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O
停止加热,将试管中的混合物冷却后倒入装有冷水的烧杯中,搅拌、静置,观察到烧杯底部有黑色物质.于是他对黑色物质进行了探究.
(2)该同学假设黑色物质是CuO.检验过程如下:
【查阅文献:检验微量Cu2+的方法是:向试液中滴加K4[Fe(CN)6]溶液,若产生红褐红沉淀,证明有Cu2+】该同学的实验操作:
①将CuO放入稀硫酸中,一段时间后,滴加K4[Fe(CN)6]溶液,产生红褐色沉淀.
②将黑色物质放入稀硫酸中,一段时间后,滴加K4[Fe(CN)6]溶液,未见红褐色沉淀.
实验①的目的是做对比实验由该检验过程所得结论是黑色沉淀中不含CuO.
(3)再次假设,黑色物质是铜的硫化物.实验如下:
 | 现象 1A试管中黑色沉淀逐渐溶解 2A试管内上方出现浅红棕色气体 3B试管中出现白色沉淀 |
②A试管上方产生浅红棕色气体的化学方程式是2NO+O2=2NO2.
③能确认黑色沉淀中含有S元素的现象是B试管中出现白色沉淀.
(4)以上实验说明,黑色物质中存在铜的硫化物.进一步实验后证明黑色物质是CuS与Cu2S的混合物.已知1molCu2S与稀硝酸反应转移8mole-,写出试管A中Cu2S溶解的化学方程式3Cu2S+20HNO3$\frac{\underline{\;\;△\;\;}}{\;}$6Cu(NO3)2+3SO2↑+8NO↑+10H2O.
分析 (1)铜和浓硫酸加热反应生成硫酸铜、二氧化硫和水;
(2)对比实验分析反应现象,判断黑色物质成分;
(3)①红棕色气体为二氧化氮,说明稀硝酸被还原生成一氧化氮,黑色固体具有还原性;
②一氧化氮与空气中的氧气反应生成红棕色的二氧化碳气体,据此写出反应的化学方程式;
③根据反应现象③可知黑色固体与稀硝酸反应生成了二氧化硫,证明黑色固体中含有硫元素;二氧化氮、二氧化硫的混合气体能够与氯化钡反应生成硫酸钡沉淀,据此写出反应的离子方程式;
④还需要确定黑色固体中含有铜离子;
(4)浓硫酸具有强氧化性,能够将硫化亚铜中硫氧化成硫酸铜、二氧化硫和水,据此写出反应的化学方程式.
解答 解:(1)铜和浓硫酸加热反应生成硫酸铜、二氧化硫和水,反应的化学方程式为:2H2SO4(浓)+Cu$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,
故答案为:2H2SO4(浓)+Cu$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;
(2)①将CuO放入稀硫酸中,一段时间后,滴加K4[Fe(CN)6]溶液,产生红褐色沉淀.
②将黑色物质放入稀硫酸中,一段时间后,滴加K4[Fe(CN)6]溶液,未见红褐色沉淀,说明黑色沉淀中不含CuO,实验①的目的是做对比实验观察反应现象,
故答案为:做对比实验;黑色沉淀中不含CuO;
(3)①A试管内上方出现红棕色气体,说明反应中有一氧化氮生成,证明了黑色固体具有还原性,在反应中被氧化,
故答案为:还原;
②红棕色气体为二氧化氮,反应的化学方程式为:2NO+O2═2NO2,
故答案为:2NO+O2═2NO2;
③根据反应现象③B试管中出现白色沉淀可知,白色沉淀为硫酸钡,说明黑色固体中含有硫元素,发生反应的离子方程式为:NO2+SO2+Ba2++H2O═BaSO4↓+NO↑+2H+,
故答案为:B试管中出现白色沉淀;
(4)浓硫酸具有强氧化性,硫化亚铜与浓硫酸反应,已知1molCu2S与稀硝酸反应转移8mole-,反应的化学方程式为:3Cu2S+2OHNO3$\frac{\underline{\;\;△\;\;}}{\;}$6Cu(NO3)2+3SO2↑+8NO↑+10H2O,
故答案为:3Cu2S+20HNO3$\frac{\underline{\;\;△\;\;}}{\;}$6Cu(NO3)2+3SO2↑+8NO↑+10H2O.
点评 本题考查了浓硫酸的化学性质、性质实验方案的设计,题目难度中等,试题涉及的题量稍大,知识点较大,理解题中信息是解题关键,如根据铜离子检验方法解答(4)④;试题培养了学生的分析、理解能力.

 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案
部分含钒物质在水中的溶解性如表所示:
| 物质 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 | HVO3 |
| 溶解性 | 可溶 | 难溶 | 难溶 | 易溶 | 难溶 |
(1)工业上常用铝热反应由V2O5冶炼金属钒,化学方程式为3V2O5+10Al$\frac{\underline{\;高温\;}}{\;}$5Al2O3+6V.
(2)反应①、②、③、④中,发生氧化还原反应的是①②(填序号),写出反应①的离子方程式V2O5+SO32-+4H+=2VO2++SO42-+2H2O.操作1、操作2用到的玻璃仪器是烧杯、玻璃棒、漏斗.
(3)反应③的沉淀率(又称沉钒率)是回收钒的关键之一,图2是反应温度与沉钒率的关系图,则控制温度的方法是将反应容器置于80℃的水浴中.

(4)反应④在焙烧过程中随温度的升高发生了两步反应.已知234gNH4VO3固体质量的减少值△W随温度(T)变化的曲线如图3.试写出300℃~350℃时反应的化学方程式2HVO3 $\frac{\underline{\;300°C-350°C\;}}{\;}$V2O5+H2O.
(5)全钒电池的电解质溶液为VOSO4溶液,电池的工作原理为VO2++V2++2H+$?_{充电}^{放电}$VO2++H2O+V3+.电池充电时阳极的电极反应式为VO2++H2O-e-=VO2++2H+.
| A. | 上述反应中氮气作还原剂 | |
| B. | 氮氧化铝中氮元素的化合价是-3 | |
| C. | 氮氧化铝晶体中的作用力是范德华力 | |
| D. | 根据氮氧化铝晶体的硬度可推断其晶体类型可能与石英相同 |
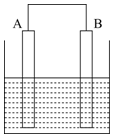
| A. | 导线中有电子流动,电流方向为A流向B | |
| B. | 溶液中的O2在电极B得电子,电极B附近碱性增强 | |
| C. | 电极A上的电极反应式为Fe-2e-=Fe2+ | |
| D. | 溶液中的Na+向电极B附近移动 |
| A. | 原电池是将化学能转变为电能的装置 | |
| B. | 构成原电池的正极和负极必须是两种不同的金属 | |
| C. | 原电池放电时,电流的方向是从正极到负极 | |
| D. | 在原电池中,电子流出的一极是负极,发生氧化反应 |
(1)电石可由焦炭与氧化钙固体在电炉中高温制得,同时生成一氧化碳气体.
①每生成1.00g固态CaC2吸收7.25kJ的热量,该制备反应的热化学方程式为CaO(s)+3C(s)$\frac{\underline{\;高温\;}}{\;}$CaC2(s)+CO(g)△H=+464kJ/mol
②CaC2与H2O反应的化学方程式为CaC2+2H2O=Ca(OH)2+HC≡CH↑
③炼钢时可用电石将钢水中FeO转变为铁,同时有一氧化碳等物质生成,该反应的化学方程式为3FeO+CaC2$\frac{\underline{\;高温\;}}{\;}$3Fe+CaO+2CO↑
(2)已知下列反应:
CH4 (g)+2O2(g)═CO2(g)+2H2O(g)△H1=akJ•mol-1
2C2H2(g)+5O2(g)═4CO2(g)+2H2O(g)△H2=bkJ•mol-1
2H2(g)+O2(g)═2H2O(g)△H3=ckJ•mol-1
2CH4(g)═C2H2(g)+3H2(g)△H4
①△H4=$\frac{4a-b-3c}{2}$kJ•mol-1(用含a、b、c的代数式表示).
②已知下列键能数据:
| 共价键 | C-H | H-H | C≡C |
| 键能/kJ•mol-1 | 413.4 | 436 | 812 |
(3)在压强为1×105kPa的恒压密闭容器中充入1mol乙炔和1molHCl气体,加入催化剂,乙炔与HCl发生反应:HC≡CH(g)+HCl(g)?CH2=CHCl(g),乙炔的平衡转化率与温度的关系如图所示:

①该反应的△H<0(填“>”或“<”),N点时乙炔的反应速率v(正)>v(逆) (填“>”、“<”或“=”).
②M点对应温度的平衡常数Kp=9.9×10-4(kPa)-1(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,并注明单位)
| A. | 反应①②中都存在:△S>0  (1)+H2(g)→ (1)+H2(g)→ (1)△H>0① (1)△H>0① | |
| B. | 反应②高温时,可自发进行 | |
| C. | 在通常情况下,①②都能自发进行 (1)+H2(g)→ (1)+H2(g)→ (1)△H<0② (1)△H<0② | |
| D. | 反应①一定不能自发进行 |

