14.分析下图所示的四个原电池装置,其中结论正确的是( )


| A. | ①②中Mg作负极,③④中Fe作负极 | |
| B. | ②中Mg作正极,电极反应式为6H2O+6e-═6OH-+3H2↑ | |
| C. | ③中Fe作负极,电极反应式为Fe-2e-═Fe2+ | |
| D. | ④中Cu作正极,电极反应式为2Cl-+2e-=Cl2↑ |
12.化学与生产生活密切相关,下列有关说法不正确的是( )
| A. | 大量使用含磷洗衣粉会造成生活污水的富营养化 | |
| B. | 用未经处理的电镀厂废水灌溉农田,易造成土壤重金属污染 | |
| C. | 臭氧一生物活性炭用于自来水深度处理,利用了活性炭的还原性 | |
| D. | 纳米铁粉可将地下水中的NO3-转化为N2,是因为纳米铁具有还原性 |
10. 某溶液中可能含有H+、Na+、NH4+、Fe3+、Al3+、SO42-、CO32-等离子.当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化的图象如图所示,下列说法不正确的是( )
某溶液中可能含有H+、Na+、NH4+、Fe3+、Al3+、SO42-、CO32-等离子.当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化的图象如图所示,下列说法不正确的是( )
 某溶液中可能含有H+、Na+、NH4+、Fe3+、Al3+、SO42-、CO32-等离子.当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化的图象如图所示,下列说法不正确的是( )
某溶液中可能含有H+、Na+、NH4+、Fe3+、Al3+、SO42-、CO32-等离子.当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化的图象如图所示,下列说法不正确的是( )| A. | 原溶液中一定含有的阳离子是H+、NH4+、Fe3+、Al3+ | |
| B. | 原溶液中一定含有SO42- | |
| C. | 原溶液中含有的Fe3+和Al3+的物质的量之比为1:1 | |
| D. | 反应最后形成的溶液中溶质为Na2SO4 |
9. 298K时,分别向体积、浓度均为20mL0.1mol•L-1的HX溶液、HY溶液中滴加等浓度的NaOH 溶液,混合溶液的pH与加入NaOH溶液体积(V)之间的关系如图所示.(注明:弱电解质的电离度等于已电离的电解质的量与电解质总量之比)下列说法正确的是( )
298K时,分别向体积、浓度均为20mL0.1mol•L-1的HX溶液、HY溶液中滴加等浓度的NaOH 溶液,混合溶液的pH与加入NaOH溶液体积(V)之间的关系如图所示.(注明:弱电解质的电离度等于已电离的电解质的量与电解质总量之比)下列说法正确的是( )
 298K时,分别向体积、浓度均为20mL0.1mol•L-1的HX溶液、HY溶液中滴加等浓度的NaOH 溶液,混合溶液的pH与加入NaOH溶液体积(V)之间的关系如图所示.(注明:弱电解质的电离度等于已电离的电解质的量与电解质总量之比)下列说法正确的是( )
298K时,分别向体积、浓度均为20mL0.1mol•L-1的HX溶液、HY溶液中滴加等浓度的NaOH 溶液,混合溶液的pH与加入NaOH溶液体积(V)之间的关系如图所示.(注明:弱电解质的电离度等于已电离的电解质的量与电解质总量之比)下列说法正确的是( )| A. | 298K 时,0.1mol•L-1HX 溶液中HX的电离度为1% | |
| B. | V=10mL时,同时微热溶液(忽略体积变化),$\frac{c({X}^{-})}{c({Y}^{-})}$逐渐增大 | |
| C. | V=20mL 时,HX曲线对应的溶液中c(Na+)=c(X-)>c(H+)=c(OH-) | |
| D. | 滴定这两种溶液时都可以选择甲基橙替代酚酞作指示剂 |
8. 常温下,向100mL 0.01mol/L HA溶液中逐滴加入0.02mol/L MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计).下列说法中,不正确的是( )
常温下,向100mL 0.01mol/L HA溶液中逐滴加入0.02mol/L MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计).下列说法中,不正确的是( )
 常温下,向100mL 0.01mol/L HA溶液中逐滴加入0.02mol/L MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计).下列说法中,不正确的是( )
常温下,向100mL 0.01mol/L HA溶液中逐滴加入0.02mol/L MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计).下列说法中,不正确的是( )| A. | HA为一元强酸 | |
| B. | MOH 为一元弱碱 | |
| C. | N点水的电离程度小于K点水的电离程度 | |
| D. | 若K点对应溶液有c(MOH)+c(M+)=2C(A_) |
7.氧化铜矿石含有CuO和Cu2(OH)2CO3,还含有Fe2O3、FeO和SiO2等.铜、铁是畜禽所必需的微量元素.某饲料厂联合生产硫酸铜和硫酸亚铁工艺流程如图1:

(1)氧化铜矿石粉碎的目的是增大接触面积,加快化学反应速率.氧化时加入的KMnO4的作用是做氧化剂.
(2)写出“酸浸”中Cu2(OH)2CO3发生反应的离子方程式Cu2(OH)2CO3+4H+=2Cu2++3H2O+CO2↑.
(3)“中和/过滤”中加入CaCO3的目的是适当降低溶液的酸性,使Fe3+水解成沉淀而除出.
(4)流程中多处涉及“过滤”,实验室中过滤操作需要使用的玻璃仪器有烧杯、玻璃棒、漏斗.
(5)加入铁屑的作用是使母液中Fe3+转化为Fe2+、除去Cu2+、提高硫酸亚铁晶体的纯度.
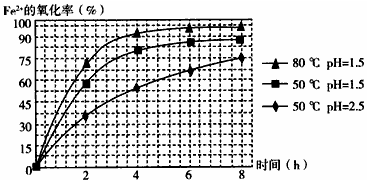
(6)表和图2“烘干粉碎”的试验结果.
硫酸铜晶体(CuSO4•5H2O)干燥实验表
表中,m为CuSO4•5H2O晶体的质量,x为干燥后所得晶体中结晶水的个数.据此可确定由CuSO4•5H2O和FeSO4•7H2O脱水得流程中所示产品的适宜工艺条件分别为160℃、3h,125(±5)℃、4.0h(分别指出两条件的温度和时间).
0 163907 163915 163921 163925 163931 163933 163937 163943 163945 163951 163957 163961 163963 163967 163973 163975 163981 163985 163987 163991 163993 163997 163999 164001 164002 164003 164005 164006 164007 164009 164011 164015 164017 164021 164023 164027 164033 164035 164041 164045 164047 164051 164057 164063 164065 164071 164075 164077 164083 164087 164093 164101 203614

(1)氧化铜矿石粉碎的目的是增大接触面积,加快化学反应速率.氧化时加入的KMnO4的作用是做氧化剂.
(2)写出“酸浸”中Cu2(OH)2CO3发生反应的离子方程式Cu2(OH)2CO3+4H+=2Cu2++3H2O+CO2↑.
(3)“中和/过滤”中加入CaCO3的目的是适当降低溶液的酸性,使Fe3+水解成沉淀而除出.
(4)流程中多处涉及“过滤”,实验室中过滤操作需要使用的玻璃仪器有烧杯、玻璃棒、漏斗.
(5)加入铁屑的作用是使母液中Fe3+转化为Fe2+、除去Cu2+、提高硫酸亚铁晶体的纯度.
(6)表和图2“烘干粉碎”的试验结果.
硫酸铜晶体(CuSO4•5H2O)干燥实验表
| 序号 | t/h | t/℃ | m/g | x |
| 1 | 3 | 80 | 5 | 4 |
| 2 | 3 | 160 | 10 | 1 |
| 3 | 4 | 160 | 10 | 0.8 |
| 4 | 4 | 160 | 5 | 0 |
| 5 | 5 | 80 | 5 | 3 |
| 6 | 5 | 160 | 15 | 1 |


 E、F、D、X、Y、Z为前四周期元素,且原子序数依次增大.E的最高正价和最低负价的绝对值相等,F有三个能级,且每个能级上的电子数相等,D原子未成对电子数在同周期元素中最多,X与D同周期,第一电离能比D低,Y与F同主族,Z的最外层只有一个电子,其它电子层电子均处于饱和状态.请回答下列问题:
E、F、D、X、Y、Z为前四周期元素,且原子序数依次增大.E的最高正价和最低负价的绝对值相等,F有三个能级,且每个能级上的电子数相等,D原子未成对电子数在同周期元素中最多,X与D同周期,第一电离能比D低,Y与F同主族,Z的最外层只有一个电子,其它电子层电子均处于饱和状态.请回答下列问题: