11.已知25℃时草酸的电离常数为K1=5.00×10-2,K2=5.40×10-5,草酸钙的Ksp=4.00×10-8,碳酸钙的Ksp=2.50×10-9.不同温度下水的离子积常数见下表:
(1)草酸在水溶液中所有的电离反应方程式H2C2O4?HC2O4-+H+,HC2O4-?C2O42-+H+;
计算25℃时KHC2O4溶液的水解平衡常数Kh=2.0×10-13;
(2)常温下将0.2mol/L的KOH溶液20mL与0.2mol/L的草酸溶液20mL混合,则混合后溶液中各离子的浓度由大到小顺序为c(K+)>c( HC2O4-)>c(H+)>c(C2O42-)>c(OH-);
(3)90℃时,将0.005mol/L的Ba(OH)2溶液20mL与0.0024mol/L的HCl溶液20mL混合,混合后溶液的pH=10;
(4)25℃时向20mL碳酸钙的饱和溶液中逐滴加入8.0×10-4mol/L的草酸钾溶液10mL,不能(填“能”或“不能”)产生沉淀.
| t/℃ | 0 | 10 | 20 | 25 | 40 | 50 | 90 | 100 |
| Kw/10-14 | 0.134 | 0.292 | 0.681 | 1.00 | 2.92 | 5.58 | 38.0 | 55.0 |
计算25℃时KHC2O4溶液的水解平衡常数Kh=2.0×10-13;
(2)常温下将0.2mol/L的KOH溶液20mL与0.2mol/L的草酸溶液20mL混合,则混合后溶液中各离子的浓度由大到小顺序为c(K+)>c( HC2O4-)>c(H+)>c(C2O42-)>c(OH-);
(3)90℃时,将0.005mol/L的Ba(OH)2溶液20mL与0.0024mol/L的HCl溶液20mL混合,混合后溶液的pH=10;
(4)25℃时向20mL碳酸钙的饱和溶液中逐滴加入8.0×10-4mol/L的草酸钾溶液10mL,不能(填“能”或“不能”)产生沉淀.
10. 某温度时,AgCl(s)?Ag+(aq)+Cl-(aq)在水中的沉淀溶解平衡曲线如图所示.下列 说法正确的是( )
某温度时,AgCl(s)?Ag+(aq)+Cl-(aq)在水中的沉淀溶解平衡曲线如图所示.下列 说法正确的是( )
 某温度时,AgCl(s)?Ag+(aq)+Cl-(aq)在水中的沉淀溶解平衡曲线如图所示.下列 说法正确的是( )
某温度时,AgCl(s)?Ag+(aq)+Cl-(aq)在水中的沉淀溶解平衡曲线如图所示.下列 说法正确的是( )| A. | 加入 AgNO3 可以使溶液由 c 点变到 d 点 | |
| B. | 加入固体 NaCl,则 AgCl 的溶解度减小,Ksp 也减小 | |
| C. | d 点有 AgCl 沉淀生成 | |
| D. | a 点对应的 Ksp小于 b 点对应的 Ksp |
9.硼砂是含结晶水的四硼酸钠,其阴离子Xm-(含B、O、H三种元素)的球棍模型如图所示,下列说法错误的是( )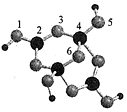

| A. | 在Xm-中,硼原子轨道的杂化类型有sp2、sp3 | |
| B. | 配位键存在于4、5原子之间 | |
| C. | m=3 | |
| D. | 硼砂晶体由Na+、Xm-和H2O构成,它们之间存在的作用力有共价键、范德华力、氢键 |
8.金属镉广泛用于合金制造及电池生产等,一种用铜镉废渣(含Cd、Zn、Cu、Fe及Co等单质)制取海绵镉的工艺流程如图:

(1)步骤Ⅰ进行破碎和粉磨的目的是提高原料浸取率和浸取时反应速率.
(2)步骤Ⅱ需隔绝O2的原因防止发生2Cu+4H++O2=2Cu2++2H2O,导致铜被浸出(用文字和方程式说明).
(3)步骤Ⅲ中除铁发生的离子反方程式为3Fe2++MnO4-+4H+=MnO2↓+3Fe3++4H2O.
(4)步骤Ⅳ调节pH适宜的试剂是ZnO或Zn(OH)2,应调整的范围为3.3~5.9.(已知部分氢氧化物开始沉淀和沉淀完全的pH如表)
(5)步骤Ⅴ发生的反应为Zn+Co2+═Zn2++Co,(已知Sb的金属活动性介于Cu和Ag之间),加入少量锑盐能加快反应的进行,其原因是形成微电池,Zn作负极,Co2+加快在锑正极表面得到电子析出;
(6)用石墨作阳极,纯锌作阴极电解ZnSO4溶液可得高纯锌,电解时总反应的离子方程式为2Zn2++2H2O $\frac{\underline{\;通电\;}}{\;}$2Zn↓+O2↑+4H+;电解后的残液返回到步骤Ⅱ(填流程中数字).

(1)步骤Ⅰ进行破碎和粉磨的目的是提高原料浸取率和浸取时反应速率.
(2)步骤Ⅱ需隔绝O2的原因防止发生2Cu+4H++O2=2Cu2++2H2O,导致铜被浸出(用文字和方程式说明).
(3)步骤Ⅲ中除铁发生的离子反方程式为3Fe2++MnO4-+4H+=MnO2↓+3Fe3++4H2O.
(4)步骤Ⅳ调节pH适宜的试剂是ZnO或Zn(OH)2,应调整的范围为3.3~5.9.(已知部分氢氧化物开始沉淀和沉淀完全的pH如表)
| 氢氧化物 | Fe(OH)3 | Cd(OH)2 | Zn(OH)2 |
| 开始沉淀的pH | 1.5 | 7.2 | 5.9 |
| 沉淀完全的pH | 3.3 | 9.9 | 8.9 |
(6)用石墨作阳极,纯锌作阴极电解ZnSO4溶液可得高纯锌,电解时总反应的离子方程式为2Zn2++2H2O $\frac{\underline{\;通电\;}}{\;}$2Zn↓+O2↑+4H+;电解后的残液返回到步骤Ⅱ(填流程中数字).
7.在密闭容器中,对于反应 N2+3H2?2NH3,在反应起始时 N2 和 H2分别为 1mol 和 3mol,当达到平衡时,N2的转化率为 30%,若以 NH3 为起始反应物,反应条件与上述反应相同,则NH3的起始的物质的量和它的转化率为( )
| A. | 4mol 35% | B. | 2mol 30% | C. | 2mol 70% | D. | 1mol 15% |
6.下列物质中含有Cl-的是( )
| A. | 液态氯化氢 | B. | 次氯酸钠溶液 | C. | 固体氯化钠 | D. | 四氯化碳 |
5.检验未知溶液中是否含有SO42-的操作合理的是( )
0 163870 163878 163884 163888 163894 163896 163900 163906 163908 163914 163920 163924 163926 163930 163936 163938 163944 163948 163950 163954 163956 163960 163962 163964 163965 163966 163968 163969 163970 163972 163974 163978 163980 163984 163986 163990 163996 163998 164004 164008 164010 164014 164020 164026 164028 164034 164038 164040 164046 164050 164056 164064 203614
| A. | 取样,加入稀硝酸酸化的Ba(NO3)2溶液 | |
| B. | 取样,先加稀硝酸酸化,再加Ba(NO3)2溶液 | |
| C. | 取样,先加盐酸酸化,再加BaCl2溶液 | |
| D. | 取样,加入盐酸酸化的BaCl2溶液 |
 已知含铜离子的颜色主要有Cu(H2O)42+(蓝色)、CuCl42-(黄色)、Cu(NH3)42+(深蓝色)等.
已知含铜离子的颜色主要有Cu(H2O)42+(蓝色)、CuCl42-(黄色)、Cu(NH3)42+(深蓝色)等.