题目内容
10. 某温度时,AgCl(s)?Ag+(aq)+Cl-(aq)在水中的沉淀溶解平衡曲线如图所示.下列 说法正确的是( )
某温度时,AgCl(s)?Ag+(aq)+Cl-(aq)在水中的沉淀溶解平衡曲线如图所示.下列 说法正确的是( )| A. | 加入 AgNO3 可以使溶液由 c 点变到 d 点 | |
| B. | 加入固体 NaCl,则 AgCl 的溶解度减小,Ksp 也减小 | |
| C. | d 点有 AgCl 沉淀生成 | |
| D. | a 点对应的 Ksp小于 b 点对应的 Ksp |
分析 A.加入 AgNO3,c(Ag+)增大,AgCl(s)?Ag+(aq)+Cl-(aq)平衡逆向移动,c(Cl-)减小;
B.Ksp与温度有关,加NaCl时溶解平衡逆向移动;
C.d 点时Qc(AgCl)>Ksp(AgCl);
D.a、b点温度相同.
解答 解:A.加入 AgNO3,c(Ag+)增大,AgCl(s)?Ag+(aq)+Cl-(aq)平衡逆向移动,c(Cl-)减小,而图中c 点变到 d 点时c(Cl-)不变,故A错误;
B.Ksp与温度有关,加NaCl时溶解平衡逆向移动,则AgCl 的溶解度减小,Ksp 不变,故B错误;
C.d 点时Qc(AgCl)>Ksp(AgCl),则d 点有 AgCl 沉淀生成,故C正确;
D.a、b点温度相同,则a点对应的 Ksp等于 b 点对应的 Ksp,故D错误;
故选C.
点评 本题考查难溶电解质的溶解平衡,为高频考点,把握图中离子浓度变化、Ksp的影响因素、沉淀的生成为解答的关键,侧重分析与应用能力的考查,注意选项B为解答的难点,题目难度不大.

练习册系列答案
相关题目
2.在一定条件下,可逆反应X(g)+3Y(g)?2Z(s)达到平衡状态的标志是( )
| A. | X、Y的浓度不再变化 | |
| B. | 单位时间生成amolX,同时生成3amolY | |
| C. | X、Y、Z的分子数之比为1:3:2 | |
| D. | X占混合气体的体积分数不变 |
3.下列物质中,不属于高分子化合物的是( )
| A. | 塑料 | B. | 淀粉 | C. | 油脂 | D. | 蛋白质 |
20.下列关于卤族元素由上到下性质递变的叙述,正确的是( )
(1)单质的氧化性增强 (2)单质的颜色加深
(3)气态氢化物的稳定性增强 (4)单质的沸点升高
(5)阴离子的还原性增强.
(1)单质的氧化性增强 (2)单质的颜色加深
(3)气态氢化物的稳定性增强 (4)单质的沸点升高
(5)阴离子的还原性增强.
| A. | (1)(2 ) (3) | B. | (2)(3)(4) | C. | (2)(4)(5) | D. | (1)(3)(5) |
5.检验未知溶液中是否含有SO42-的操作合理的是( )
| A. | 取样,加入稀硝酸酸化的Ba(NO3)2溶液 | |
| B. | 取样,先加稀硝酸酸化,再加Ba(NO3)2溶液 | |
| C. | 取样,先加盐酸酸化,再加BaCl2溶液 | |
| D. | 取样,加入盐酸酸化的BaCl2溶液 |
2.某有机物的结构简式如图,下列结论正确的是( )
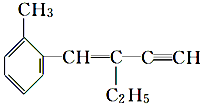

| A. | 该有机物结构简式为C13H14 | |
| B. | 该有机物属于苯的同系物 | |
| C. | 该有机物分子中至少有6个碳原子共平面 | |
| D. | 该有机物能与溴水发生加成反应且1mol该有机物最多能加成3mol的Br2 |
20.下列说法不正确的是( )
| A. | 燃烧煤炭供热会加剧“温室效应“ | |
| B. | 将废旧电池深埋处理,可有效防止电池中的重金属污染 | |
| C. | 预防H7N9流感病毒的措施之一是高温消毒餐具等生活日用品 | |
| D. | 开发利用太阳能、风能、生物能、海洋能等清洁能源,符合“低碳经济” |
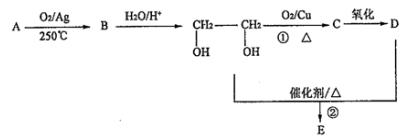
 .
.