题目内容
9.硼砂是含结晶水的四硼酸钠,其阴离子Xm-(含B、O、H三种元素)的球棍模型如图所示,下列说法错误的是( )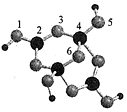
| A. | 在Xm-中,硼原子轨道的杂化类型有sp2、sp3 | |
| B. | 配位键存在于4、5原子之间 | |
| C. | m=3 | |
| D. | 硼砂晶体由Na+、Xm-和H2O构成,它们之间存在的作用力有共价键、范德华力、氢键 |
分析 结合化合价代数和为0的原则判断m的值,1,3,5,6代表氧原子,2,4代表B原子,2号B形成3个键,则B原子为SP2杂化,4号B形成4个键,则B原子为SP3杂化; B一般是形成3个键,4号B形成4个键,其中1个键很可能就是配位键,配位键存在4号与5号之间;钠离子与Xm-形成离子键,结晶水分子间存在氢键和范德华力分析判断.
解答 解:A.1,3,5,6代表氧原子,2,4代表B原子,2号B形成3个键,则B原子为SP2杂化,4号B形成4个键,则B原子为SP3杂化,故A正确;
B.B一般是形成3个键,4号B形成4个键,其中1个键很可能就是配位键,配位键存在4号与5号之间,故B正确;
C.观察模型,可知Xm-是(H4B4O9)m-,依据化合价H为+1,B为+3,O为-2,可得m=2,故C错误;
D.硼砂晶体由Na+、Xm-和H2O构成,Na+、Xm-之间存在离子键,结晶水分子间存在氢键和范德华力,水分子中存在共价键,故D正确;
故选C.
点评 本题考查了晶胞的结构、杂化类型的判断、化学键和氢键,题目综合性较强,题目难度中等,侧重于考查学生的分析能力和应用能力,注意对球棍模型的分析应用.

练习册系列答案
相关题目
1.如图所示的原电池装置,下列判断正确的是( )


| A. | 外电路的电流方向为:X→导线→Y | |
| B. | 若两电极都是金属,则它们的活动性顺序为X<Y | |
| C. | X极上发生的是还原反应,Y极上发生的是氧化反应 | |
| D. | 放电一段时间后,烧杯中溶液的酸性减弱 |
19.氢化铵(NH4H)与氯化铵的结构相似,已知NH4H与水反应有H2生成,下列叙述不正确的是( )
| A. | NH4H是离子化合物,含有离子键和共价键 | |
| B. | NH4H溶于水,所形成的溶液显碱性 | |
| C. | NH4H与水反应时,NH4H是氧化剂 | |
| D. | 将NH4H固体投入少量水中,有两种气体产生 |
1.除去下列物质中杂质(括号内为杂质),所选用试剂及操作方法不正确一组( )
| 选项 | 待提纯的物质 | 选用试剂 | 操作的方法 |
| A | FeCl3溶液(FeCl2溶液) | Cl2 | -- |
| B | Al2O3(Fe2O3) | NaOH溶液和CO2 | 溶解、过滤、过滤 |
| C | Cl2(HCl) | 饱和食盐水 | 洗气 |
| D | CO2(SO2) | 酸性KMnO4溶液 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
18.下列反应能用 H++HCO3-=H2O+CO2↑的离子方程式表示的反应是( )
| A. | 碳酸氢钠溶液和稀硫酸的反应 | B. | 碳酸氢钠溶液和醋酸溶液的反应 | ||
| C. | 碳酸氢钾溶液和醋酸溶液的反应 | D. | 碳酸氢钡溶液与稀硫酸的反应 |
19. 在10L的密闭容器中,A、B、C 三种物质的物质的量(n)与时间(t)的关系如图一所示,C的百分含量(C%)与温度(T)的关系如图二所示,下列分析错误的是( )
在10L的密闭容器中,A、B、C 三种物质的物质的量(n)与时间(t)的关系如图一所示,C的百分含量(C%)与温度(T)的关系如图二所示,下列分析错误的是( )
 在10L的密闭容器中,A、B、C 三种物质的物质的量(n)与时间(t)的关系如图一所示,C的百分含量(C%)与温度(T)的关系如图二所示,下列分析错误的是( )
在10L的密闭容器中,A、B、C 三种物质的物质的量(n)与时间(t)的关系如图一所示,C的百分含量(C%)与温度(T)的关系如图二所示,下列分析错误的是( )| A. | 该反应的化学方程式是2A+B?C | |
| B. | 0~4 min时,A的平均反应速率为0.1 mol/(L•min) | |
| C. | 由T1向T2变化时,v(正)>v(逆) | |
| D. | 平衡后升高温度,反应的平衡常数K值减小 |
 )中标有“*’’的碳原子即为手性碳原子.
)中标有“*’’的碳原子即为手性碳原子. 或
或 .
. 已知含铜离子的颜色主要有Cu(H2O)42+(蓝色)、CuCl42-(黄色)、Cu(NH3)42+(深蓝色)等.
已知含铜离子的颜色主要有Cu(H2O)42+(蓝色)、CuCl42-(黄色)、Cu(NH3)42+(深蓝色)等. ⑤
⑤ ⑥
⑥ ⑦
⑦
 ⑨CCl2F2⑩CCl4⑪CH3CH2OH⑫
⑨CCl2F2⑩CCl4⑪CH3CH2OH⑫