9.分子式为C4H9OCl,且能与钠反应产生氢气的有机物可能的同分异构体(不考虑立体异构)数目为( )
| A. | 9 | B. | 10 | C. | 11 | D. | 12 |
8. 现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍:Y与Z能形成Z2Y、Z2Y2 型离子化合物,Z与T形成的Z2T化合物能破坏水的电离平衡.六种元素的原子半径与原子序数的关系如图所示.下列推断不正确的是( )
现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍:Y与Z能形成Z2Y、Z2Y2 型离子化合物,Z与T形成的Z2T化合物能破坏水的电离平衡.六种元素的原子半径与原子序数的关系如图所示.下列推断不正确的是( )
 现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍:Y与Z能形成Z2Y、Z2Y2 型离子化合物,Z与T形成的Z2T化合物能破坏水的电离平衡.六种元素的原子半径与原子序数的关系如图所示.下列推断不正确的是( )
现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍:Y与Z能形成Z2Y、Z2Y2 型离子化合物,Z与T形成的Z2T化合物能破坏水的电离平衡.六种元素的原子半径与原子序数的关系如图所示.下列推断不正确的是( )| A. | Y、Z组成的化合物只含离子键 | |
| B. | 氢化物的沸点和稳定性排序:R<Y | |
| C. | 最高价氧化物对应的水化物的酸性:T>R | |
| D. | 由X、Y、Z、T四种元素组成的化合物水溶液一定显酸性 |
7.气体分子中的极性键在红外线的照射下,会像弹簧一样做伸缩和弯曲运动,从而产生热量.下列气体的分子中不存在极性键的是( )
| A. | CO2 | B. | SO2 | C. | CH4 | D. | N2 |
6.化学在工业生产方面有着广泛的应用,主要通过技术创新和改进,生产各种化学品.在下列化工生产中,发生的主要反应不涉及化学变化的是( )
| A. | 石油分馏 | B. | 乙烯制聚乙烯 | C. | 工业冶炼铁 | D. | 从海水中提取镁 |
5.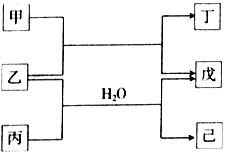 短周期元素E、R、X、Y、Z的原子序数依次增大,它们组成的单质或化合物存在如下转化关系,甲、丁为二元化合物,乙、戊为单质,丙、己为三元化合物.已知25℃时,0.1mol•L-1甲、丙两溶液的pH分别为1、13,丁、己两溶液混合时产生白色沉淀.下列说法正确的是( )
短周期元素E、R、X、Y、Z的原子序数依次增大,它们组成的单质或化合物存在如下转化关系,甲、丁为二元化合物,乙、戊为单质,丙、己为三元化合物.已知25℃时,0.1mol•L-1甲、丙两溶液的pH分别为1、13,丁、己两溶液混合时产生白色沉淀.下列说法正确的是( )
 短周期元素E、R、X、Y、Z的原子序数依次增大,它们组成的单质或化合物存在如下转化关系,甲、丁为二元化合物,乙、戊为单质,丙、己为三元化合物.已知25℃时,0.1mol•L-1甲、丙两溶液的pH分别为1、13,丁、己两溶液混合时产生白色沉淀.下列说法正确的是( )
短周期元素E、R、X、Y、Z的原子序数依次增大,它们组成的单质或化合物存在如下转化关系,甲、丁为二元化合物,乙、戊为单质,丙、己为三元化合物.已知25℃时,0.1mol•L-1甲、丙两溶液的pH分别为1、13,丁、己两溶液混合时产生白色沉淀.下列说法正确的是( )| A. | 原子半径的大小Z>Y>X>R>E | |
| B. | X、Y、Z的最高价氧化物对应的水化物能相互反应 | |
| C. | E、R、Z三种元素不可能存在于同一种共价化合物中 | |
| D. | Z的阴离子夺取质子的能力较R的阴离子强 |
4.下列叙述Ⅰ、Ⅱ正确且有因果关系的是( )
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | 金属钠具有强还原性 | 金属钠可制作高压钠灯 |
| B | Al2O3是两性氧化物 | Al2O3可用作耐火材料 |
| C | 明矾溶于水生成Al(OH)3胶体 | 明矾可作净水剂 |
| D | Fe2O3是碱性氧化物 | Fe2O3可作红色油漆和涂料 |
| A. | A | B. | B | C. | C | D. | D |
3.下列说法正确的是( )
| A. | 原子的电子层数越多,原子半径一定越大 | |
| B. | 卤族元素的单质均有氧化性,最高正价都是+7 | |
| C. | 同族元素相差的原子序数可能为16、26、36、46 | |
| D. | ⅠA族与ⅦA族元素间可形成共价化合物或离子化合物 |
2.下列化学用语表达正确的是( )
| A. | 氮气的电子式  | B. | 苯分子的实验式为CH | ||
| C. | 次氯酸的电子式  | D. | 乙烯的结构简式 CH2CH2 |
1.下列叙述正确的是( )
| A. | 根据核磁共振氢谱不能鉴别1-溴丙烷和2-溴丙烷 | |
| B. | 沸点:CH3CH3>CH3CH2OH;密度: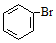 > >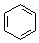 | |
| C. | 苯酚钠溶液中通入少量的CO2离子方程式为:C6H5O-+H2O+CO2→C6H5OH+CO32- | |
| D. | 要检验溴乙烷中的溴元素,向其中加入NaOH溶液共热,冷却后先加硝酸酸化,再加入硝酸银溶液,观察有无浅黄色沉淀生成 |
20.化学与生产、生活密切相关.下列叙述正确的是( )
0 163728 163736 163742 163746 163752 163754 163758 163764 163766 163772 163778 163782 163784 163788 163794 163796 163802 163806 163808 163812 163814 163818 163820 163822 163823 163824 163826 163827 163828 163830 163832 163836 163838 163842 163844 163848 163854 163856 163862 163866 163868 163872 163878 163884 163886 163892 163896 163898 163904 163908 163914 163922 203614
| A. | 煤的干馏和石油的分馏均属化学变化 | |
| B. | 用浸泡过高锰酸钾溶液的硅藻土吸收水果释放的乙烯,可到达水果保鲜的目的 | |
| C. | 天然药物无任何毒副作用,可长期服用 | |
| D. | 可以用灼烧的方法鉴别羊毛和蚕丝 |