9. 已知:T℃时,Ksp(CaSO4)=4.90×10-5、Ksp(CaCO3)=2.8×10-9、Ksp(PbCO3)=8.4×10-14,三种盐的沉淀溶解平衡曲线如图所示,pM=-lgc(阴离子)、pN=-lgc(阳离子).下列说法正确的是( )
已知:T℃时,Ksp(CaSO4)=4.90×10-5、Ksp(CaCO3)=2.8×10-9、Ksp(PbCO3)=8.4×10-14,三种盐的沉淀溶解平衡曲线如图所示,pM=-lgc(阴离子)、pN=-lgc(阳离子).下列说法正确的是( )
 已知:T℃时,Ksp(CaSO4)=4.90×10-5、Ksp(CaCO3)=2.8×10-9、Ksp(PbCO3)=8.4×10-14,三种盐的沉淀溶解平衡曲线如图所示,pM=-lgc(阴离子)、pN=-lgc(阳离子).下列说法正确的是( )
已知:T℃时,Ksp(CaSO4)=4.90×10-5、Ksp(CaCO3)=2.8×10-9、Ksp(PbCO3)=8.4×10-14,三种盐的沉淀溶解平衡曲线如图所示,pM=-lgc(阴离子)、pN=-lgc(阳离子).下列说法正确的是( )| A. | a线代表的是PbCO3 | |
| B. | T℃时,向10 mL水中加入CaCO3和PbCO3至二者均饱和,溶液中c(Ca2+):c(Pb2+)=3×10-5 | |
| C. | d点可以代表CaCO3的饱和溶液,且c(Ca2+)=c(CO32-) | |
| D. | T℃时,向CaCO3悬浊液中加入NH4Cl固体,会使图象中d点向f点转化 |
7.下列物质中,有非极性键的共价化合物是⑩;既有离子键又有非极性键的是④.(填序号)
①I2 ②H2 ③NH4NO3 ④K2 O2 ⑤Ba(OH)2 ⑥CH4 ⑦CO2 ⑧NaF ⑨NH3⑩H2 O2.
①I2 ②H2 ③NH4NO3 ④K2 O2 ⑤Ba(OH)2 ⑥CH4 ⑦CO2 ⑧NaF ⑨NH3⑩H2 O2.
4.某烃与H21:1加成后产物是 ,则该径的结构可能有( )
,则该径的结构可能有( )
 ,则该径的结构可能有( )
,则该径的结构可能有( )| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
2.为研究沉淀的生成及其转化,某小组进行如下实验.关于该实验的分析不正确的是( )

| A. | ①浊液中存在平衡:Ag2CrO4(s)?2Ag+(aq)+CrO42-(aq) | |
| B. | ②中溶液变澄淸原因:AgOH+2NH3•H2O═[Ag(NH3)2]OH+2H2O | |
| C. | ③中顔色变化说明有AgCl生成 | |
| D. | 该实验可以证明AgCl比Ag2CrO4更难溶 |
1. 常温下,向 1L 0.10mol•L-1CH3COONa 溶液中,不断通入HC1气体(忽略溶液体积变化),得到 c (CH3COO-)和c(CH3COOH)与 pH 的变化关系如下,则下列说法正确的是( )
常温下,向 1L 0.10mol•L-1CH3COONa 溶液中,不断通入HC1气体(忽略溶液体积变化),得到 c (CH3COO-)和c(CH3COOH)与 pH 的变化关系如下,则下列说法正确的是( )
0 163690 163698 163704 163708 163714 163716 163720 163726 163728 163734 163740 163744 163746 163750 163756 163758 163764 163768 163770 163774 163776 163780 163782 163784 163785 163786 163788 163789 163790 163792 163794 163798 163800 163804 163806 163810 163816 163818 163824 163828 163830 163834 163840 163846 163848 163854 163858 163860 163866 163870 163876 163884 203614
 常温下,向 1L 0.10mol•L-1CH3COONa 溶液中,不断通入HC1气体(忽略溶液体积变化),得到 c (CH3COO-)和c(CH3COOH)与 pH 的变化关系如下,则下列说法正确的是( )
常温下,向 1L 0.10mol•L-1CH3COONa 溶液中,不断通入HC1气体(忽略溶液体积变化),得到 c (CH3COO-)和c(CH3COOH)与 pH 的变化关系如下,则下列说法正确的是( )| A. | 溶液的pH比较:x<y<z | |
| B. | 在y点再通入0.05 mol HCl气体,溶液中离子浓度大小比较:c(Na+)=c(Cl-)>c(H+)>c(CH3COO-)>c(OH-) | |
| C. | 在溶液中加入一滴强酸或强碱,溶液pH变化最小的是y点 | |
| D. | 该温度下,CH3COOH的Ka=104.75 |

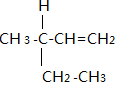
 .
.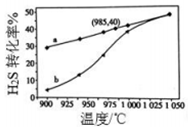 废气中的H2S通过高温热分解可制取氢气:2H2S(g)?2H2(g)+S2(g).在3L密闭容器中,控制不同温度进行H2S分解实验.
废气中的H2S通过高温热分解可制取氢气:2H2S(g)?2H2(g)+S2(g).在3L密闭容器中,控制不同温度进行H2S分解实验.