3.若NA表示阿伏加德罗常数,下列说法中正确的是( )
| A. | 1.6gCH4与1.8gNH4+所含质子数均为NA | |
| B. | 常温下,5.6g铁钉与足量浓硝酸反应,转移的电子数为0.3NA | |
| C. | 0.5 mol•L-1Na2CO3溶液中,阴阳离子总数为1.5NA | |
| D. | 常温常压下,44gCO2气体中所含的分子数为NA |
2.下列离子方程式正确的是( )
| A. | 成分为盐酸的洁厕灵与84消毒液混合使用易中毒:Cl-+ClO-+2H+=Cl2↑+H2O | |
| B. | Na2O2与H2O反应:2O22-+2H2O=4OH-+O2↑ | |
| C. | NaHSO4溶液中滴入少量Ba(OH)2:H++SO42-+Ba2++OH-=BaSO4↓+H2O | |
| D. | FeI2溶液中滴入过量溴水:2Fe2++2I-+2Br2=2Fe3++I2+4Br- |
1.现有两个热化学方程式:下列说法中正确的是( )


| A. | 反应①②中都存在:△S>0 | B. | 反应②高温时,可自发进行 | ||
| C. | 在通常情况下,①②都能自发进行 | D. | 反应①一定不能自发进行 |
19.亚硝酰氯(NOC1)是有机合成中的重要试剂,可由NO和Cl2反应得到,化学方程式为 2NO(g)+Cl2(g)=2NOCl(g).
(1)已知几种化学键的键能数据如下表(亚硝酸氯的结构式为Cl-N=0):
则 2N0(g)+Cl2(g)=2NOCl(g)△H=289-2aKJ•mol-1 (用含a 的式子表示).
(2)300℃时,在恒容密闭容器中发生反应:2NOC1(g)═2NO(g)+Cl2(g).该反应速率的表达式为v正=k•cn(NOCl)(k为速率常数,只与温度有关),正反应速率与浓度的关系如表所示:
计算:n=2,k=4.0×10-7mol-1•L•s-1.
(3)在2L恒容密闭容器中充入4mo1NO(g)和2mol Cl2(g),f发生反应2NO(g)+Cl2(g)═2NOCl (g).在不同温度下c(NOCl)与时间t的关系如图Ⅰ所示:

①判断:Tl<T2;此反应的△H<0 (两空均填“>”“<”或“=”).
②反应开始到lOmin时平均反应速率v(NO)=0.1mol•L-1•min-1.
③T2时此反应的平衡常数K=2L/mol.
(4)在密闭容器中充入NO(g)和Cl2(g),发生反应2NO(g)+Cl2(g)-2NOCl(g).改变外界条件X,NO的转化率变化关系如图Ⅱ所示,则X可能是BC(填标号).
A.温度 B.压强C.$\frac{n(C{l}_{2})}{n(NO)}$ D.与催化剂的接触面积.
(1)已知几种化学键的键能数据如下表(亚硝酸氯的结构式为Cl-N=0):
则 2N0(g)+Cl2(g)=2NOCl(g)△H=289-2aKJ•mol-1 (用含a 的式子表示).
(2)300℃时,在恒容密闭容器中发生反应:2NOC1(g)═2NO(g)+Cl2(g).该反应速率的表达式为v正=k•cn(NOCl)(k为速率常数,只与温度有关),正反应速率与浓度的关系如表所示:
| 序号 | c(NOCl)/mol•L-1 | v/mol•L-1•S-1 |
| ① | 0.30 | 3.60×10-9 |
| ② | 0.60 | 1.44×10-8 |
| ③ | 0.90 | 3.24×10-8 |
| 化学键 | NO中的氮氧键 | Cl-C1 键 | C1-N 键 | N0C1中的N=0键 |
| 键能/KJ•mol-1 | 630 | 243 | a | 607 |

①判断:Tl<T2;此反应的△H<0 (两空均填“>”“<”或“=”).
②反应开始到lOmin时平均反应速率v(NO)=0.1mol•L-1•min-1.
③T2时此反应的平衡常数K=2L/mol.
(4)在密闭容器中充入NO(g)和Cl2(g),发生反应2NO(g)+Cl2(g)-2NOCl(g).改变外界条件X,NO的转化率变化关系如图Ⅱ所示,则X可能是BC(填标号).
A.温度 B.压强C.$\frac{n(C{l}_{2})}{n(NO)}$ D.与催化剂的接触面积.
18. 一定条件下,体积为10L的固定容器发生反应:N2(g)+3H2(g)?2NH3(g)△H<0,反应过程如图:下列说法正确的是( )
一定条件下,体积为10L的固定容器发生反应:N2(g)+3H2(g)?2NH3(g)△H<0,反应过程如图:下列说法正确的是( )
 一定条件下,体积为10L的固定容器发生反应:N2(g)+3H2(g)?2NH3(g)△H<0,反应过程如图:下列说法正确的是( )
一定条件下,体积为10L的固定容器发生反应:N2(g)+3H2(g)?2NH3(g)△H<0,反应过程如图:下列说法正确的是( )| A. | t1min时正、逆反应速率相等 | |
| B. | X曲线表示NH3的物质的量随时间变化的关系 | |
| C. | 0~8 min,H2的平均反应速率 v(H2)=0.075mol•L-1•min-1 | |
| D. | 10~12 min,升高温度使反应速率加快,平衡正向移动 |
15.锰酸锂(LiMn2O4)可作为锂离子电池的正极材料,在工业上可利用软锰矿浆(主要成分为MnO2,含少量Fe2O3、FeO、Al2O3、SiO2制备锰酸锂,生产流程如图1:
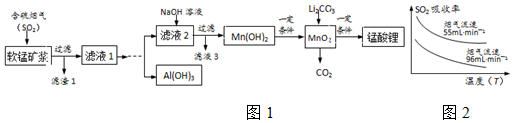
已知:
①软锰矿浆在吸收含硫烟气的过程中酸性逐渐增强.
②在此流程中部分金属阳离子生成氢氧化物沉淀的pH如表:
(1)已知:SO2的吸收率与温度及烟气流速的关系如图2.为提高含硫烟气中SO2的吸收率,可以采取的措施
降低通入含硫烟气的温度或减小通入含硫烟气的流速
(2)滤液1中所含金属阳离子有Mn2+、Al3+、Fe2+(填离子符号).
(3)在实际生产中,在实际生产中,Li2CO3与MnO2按物质的量之比为1:4混合均匀加热制取LiMn2O4.
①升温到515℃时,Li2CO3开始分解产生CO2,同时生成固体A,此时比预计Li2CO3的分解温度(723℃)低得多,可能原因是MnO2对Li2CO3的分解有催化剂的作用
②升温到566℃时,MnO2开始分解产生另一种气体X,X恰好与①中产生的CO2物质的量相等,同时得到固体B.请写出此过程发生的化学反应方程式4MnO2 $\frac{\underline{\;566℃\;}}{\;}$2Mn2O3+O2↑
③升温到720℃时,A、B反应,固体质量逐渐增加,当质量不再增加时,得到高纯度的锰酸锂.请写出发生的化学反应方程式2Li2O+4Mn2O3+O2$\frac{\underline{\;720℃\;}}{\;}$4LiMn2O4
(4)请补充完整由“滤液1”得到“滤液2”和Al(OH)3的实验方案[Al(OH)3在pH≥12时溶解]:边搅拌边向滤液1中滴加足量过氧化氢,搅拌加入氢氧化钠溶液至4.7≤PH<7.7,过滤得到滤液2和固体向所得固体中加入氢氧化钠溶液至PH≥12,搅拌过滤再向所得滤液中通入二氧化碳过滤洗涤,低温烘干得到氢氧化铝(实验中须用到的试剂有:NaOH溶液、H2O2、CO2)

已知:
①软锰矿浆在吸收含硫烟气的过程中酸性逐渐增强.
②在此流程中部分金属阳离子生成氢氧化物沉淀的pH如表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 3.4 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 4.7 | 9.8 |
降低通入含硫烟气的温度或减小通入含硫烟气的流速
(2)滤液1中所含金属阳离子有Mn2+、Al3+、Fe2+(填离子符号).
(3)在实际生产中,在实际生产中,Li2CO3与MnO2按物质的量之比为1:4混合均匀加热制取LiMn2O4.
①升温到515℃时,Li2CO3开始分解产生CO2,同时生成固体A,此时比预计Li2CO3的分解温度(723℃)低得多,可能原因是MnO2对Li2CO3的分解有催化剂的作用
②升温到566℃时,MnO2开始分解产生另一种气体X,X恰好与①中产生的CO2物质的量相等,同时得到固体B.请写出此过程发生的化学反应方程式4MnO2 $\frac{\underline{\;566℃\;}}{\;}$2Mn2O3+O2↑
③升温到720℃时,A、B反应,固体质量逐渐增加,当质量不再增加时,得到高纯度的锰酸锂.请写出发生的化学反应方程式2Li2O+4Mn2O3+O2$\frac{\underline{\;720℃\;}}{\;}$4LiMn2O4
(4)请补充完整由“滤液1”得到“滤液2”和Al(OH)3的实验方案[Al(OH)3在pH≥12时溶解]:边搅拌边向滤液1中滴加足量过氧化氢,搅拌加入氢氧化钠溶液至4.7≤PH<7.7,过滤得到滤液2和固体向所得固体中加入氢氧化钠溶液至PH≥12,搅拌过滤再向所得滤液中通入二氧化碳过滤洗涤,低温烘干得到氢氧化铝(实验中须用到的试剂有:NaOH溶液、H2O2、CO2)
14.下列装置或操作不能达到实验目的是( )
0 163539 163547 163553 163557 163563 163565 163569 163575 163577 163583 163589 163593 163595 163599 163605 163607 163613 163617 163619 163623 163625 163629 163631 163633 163634 163635 163637 163638 163639 163641 163643 163647 163649 163653 163655 163659 163665 163667 163673 163677 163679 163683 163689 163695 163697 163703 163707 163709 163715 163719 163725 163733 203614
| A. |  装置关闭止水夹,往长颈漏斗加水,根据水位的变化情况可检查该装置的气密性 | |
| B. | 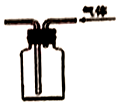 装置可用来收集NH3、H2等 | |
| C. |  装置可用来吸收极易溶于水的气体如NH3、HCl等 | |
| D. |  装置洗涤沉淀物时,向漏斗中加蒸馏水至浸没沉淀物,滤出溶液并重复操作2-3次 |

